2025年第4

摩熵咨询医药行业观察周报(2025.01.20-2025.02.02)
摩熵咨询医药行业观察周报(2025.01.20-2025.02.02)
*本文内容节选自摩熵咨询医药行业观察周报(2025.01.20-2025.02.02),若您对全文感兴趣,欢迎下载完整报告!
摩熵咨询
创新药/改良型新药 仿制药 行业政策法规
21页
1.3.1本周国内医药大健康行业政策法规速览
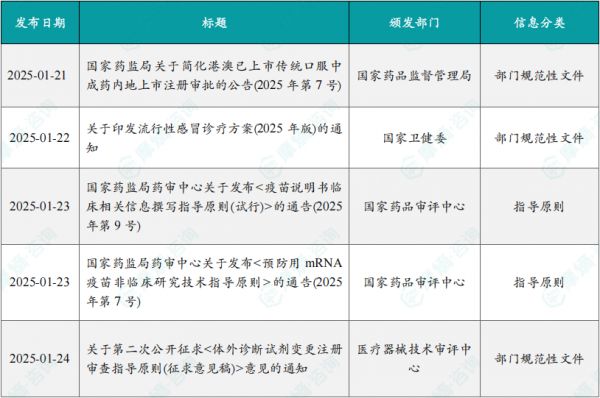
1.3.2本周重点行业政策详细说明
(1)《国家药监局关于简化港澳已上市传统口服中成药内地上市注册审批的公告》
1月21日,为贯彻落实国家建设粤港澳大湾区战略部署,进一步支持香港特别行政区、澳门特别行政区(以下简称香港、澳门特区)中医药事业发展,更好融入国家发展大局,国家药监局发布了《国家药监局关于简化港澳已上市传统口服中成药内地上市注册审批的公告(2025年第7号)》。
政策允许港澳已上市15年以上的传统口服中成药在内地直接申请上市,并认可其在港澳的试验研究资料和人用经验总结,大幅缩短了审批时间,降低了企业成本。这不仅有助于推动港澳中医药产业的创新发展,也为内地患者提供了更多安全有效的传统中成药选择。同时,政策明确了上市后监管责任,确保药品质量和安全,为粤港澳大湾区中医药产业的高质量发展提供了有力支持。
(2)国家药监局药审中心关于发布《疫苗说明书临床相关信息撰写指导原则(试行)》的通告
1月23日,为加强说明书的规范管理,指导疫苗上市许可持有人规范撰写疫苗说明书,在国家药品监督管理局的部署下,药审中心组织制定了《疫苗说明书临床相关信息撰写指导原则(试行)》。疫苗作为公共卫生领域的重要产品,关系到广大人民群众的健康,因此,准确的说明书对于医生、患者以及药品监管部门至关重要。
该指导原则的作用在于通过统一标准,确保疫苗说明书中的临床数据和使用说明具备科学性和一致性,避免因信息不充分或表达不清造成误导或用药不当。对于疫苗上市许可持有人来说,该政策为其提供了明确的撰写框架和要求,促进了疫苗产品的规范化管理。此外,统一的说明书要求有助于提高疫苗的透明度,增强公众对疫苗安全性的信任。
同期事件:
1. 2025年第4-5周01.20-02.02国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2025年第4-5周01.20-02.02国内仿制药/生物类似物申报/审批数据分析
3. 2025年第4-5周01.20-02.02全球创新药研发概览
以上内容均来自{摩熵咨询医药行业观察周报(2025.01.20-2025.02.02)},如需查看或下载完整版报告,可点击!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>
*声明:本文由入驻摩熵医药的相关人员撰写或转载,观点仅代表作者本人,不代表摩熵医药的立场。
相关知识
2025年4月25
2025年4月13日
2025年高考第四节生物的变异
富士康布局 AR 新赛道,计划 2025 年第4季度量产 Micro LED 晶圆
2025年4月22日适合买狗吗 2025年4月22日是买狗的黄道吉日吗
2025年第一弹—用DeepSeek制定减肥计划
2025年4月健康防护提示
今日辟谣(2025年3月4日)
2025年企模
新年,2025年的第一条“朋友圈”该怎么发?看看“这5条”如何?
网址: 2025年第4 https://m.trfsz.com/newsview1289552.html