眼压计注册技术审查指导原则
本指导原则旨在指导注册申请人对眼压计产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是对眼压计产品的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是供申请人和审查人员使用的指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规、标准体系及当前认知水平下制定的,随着法规、标准体系的不断完善和科学技术的不断发展,本指导原则相关内容也将适时进行调整。
一、适用范围
本指导原则适用于非接触式眼压计和回弹式眼压计,根据《医疗器械分类目录》(国家食品药品监督管理总局公告2017年第104号),眼压计产品按二类医疗器械管理,分类编码为16—04—17(眼科器械—眼科测量诊断设备和器具—眼压计)。
本指导原则范围不包含机械式眼压计。
二、技术审查要点
(一)产品名称要求
眼压计产品的命名应符合国家关于医疗器械命名规则的要求,名称中的核心词一般为眼压计,特征词中可体现接触形式或测试方式等内容。如:非接触式眼压计、回弹式眼压计等。产品名称应为通用名,不应包括产品型号、系列。
(二)产品的结构和组成
非接触式眼压计一般为台式,由主机和电源线构成,其中主机包括显示模块、喷气模块、光路系统、计算处理单元、控制单元、三维运动系统。其中光路系统一般包括对准模块和检测模块。
产品结构框图如图1所示。
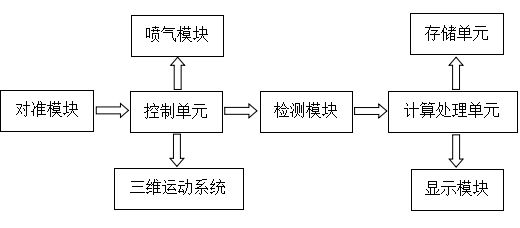
图 1 非接触式眼压计产品结构框图
回弹式眼压计一般为手持式,由驱动线圈(可包含探针)、控制单元、计算处理单元、显示模块组成。产品结构框图如图2所示。
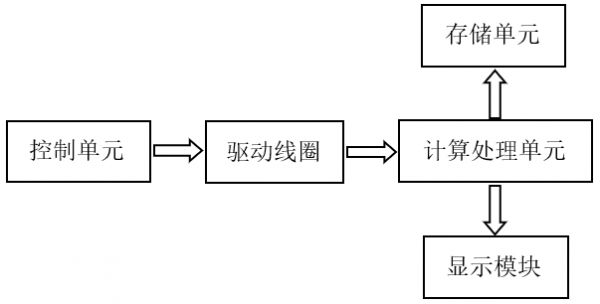
图 2 回弹式眼压计产品结构框图
图3中给出了两种眼压计产品的图示举例,供审查人员参考。

图 3 眼压计产品图示举例
(三)产品工作原理/作用机理
非接触式眼压计的原理是利用一种可控的空气脉冲,其压力具有线性增加的特性,即喷射空气的力量随时间的延长呈线性增加。通过喷气模块将气体喷射到角膜中央表面,使角膜产生形变,形成一个直径3.6mm的圆形平面。依照Limber-Fick定律,此时角膜上的空气压力与人眼内压相等。系统可以通过气路中的压力传感器得出此时的空气压力,即人眼内压数值。
非接触式眼压计将一束光投射到角膜上。该光束经过角膜的反射后被检测模块中的光电探测器接收。光电探测器将接收的光信号转化为电信号,被系统监测。随着角膜形变的增加,光电探测器上接收的光能量也随之增加,直至压平角膜的面积达到3.6mm直径时,其接收到的光能量也达到了最大值。此时压力传感器测得的空气压力等于人眼内压数值。图4给出了眼压测试过程中光电探测器信号、压力传感器信号和气
相关知识
眼压计注册技术审查指导原则
[CMDE]关于公开征求《面部注射填充材料临床试验注册审查指导原则(征求意见稿)》等医疗器械注册审查指导原则意见的通知
食药监总局解读《医疗器械网络安全注册技术审查指导原则》
食品药品监管总局发布医疗器械网络安全注册技术审查指导原则
医疗器械网络安全注册审查指导原则(2022年修订版) – ReguVerse
国家药监局发布医疗器械网络安全注册审查指导原则(2022年修订版)的通告(2022年第7号)
《保健食品及其原料安全性毒理学检验与评价技术指导原则(2020年版)》解读
体重控制药物临床试验技术指导原则
ISO45001职业健康安全管理体系OHSMS国家注册审核员人员注册准则
安全性评价研究中心 指导原则 预防用生物制品临床前安全性评价技术审评一般原则
网址: 眼压计注册技术审查指导原则 https://m.trfsz.com/newsview1401238.html