下一代RNA赛道:资本泡沫还是产业机遇?
前言 过去十年基于多种RNA技术的药物(如RNA干扰和反义寡核苷酸)已经上市,同时,下一代RNA(如环状RNA和tRNA)在新冠mRNA疫苗产业的带动下弯道超车,掀起了另一波关注,成为近两年全球医药领域关注的焦点和投融资的风口。
常见的各类RNA分子(图片来源:Whitehead Institute)
下一代RNA技术代表着一种发展迅速,可用于治疗广泛疾病领域的颠覆性治疗模式。虽然尚处于早期,需要多年研究,但初创公司已从世界级的风险投资机构、大型医药公司和其他投资集团筹集了高额资金。 2022年8月16日,默沙东宣布与环状RNA领先企业Orna Therapeutics公司达成合作,下一代RNA赛道再度吸金超36亿美金。 此外,多家中国企业也有布局,技术上和部分管线与国际企业齐头并进。 本文我们对两种相对较新、受资本高度关注的RNA疗法——环状RNA和tRNA进行了整理研究,分析和展望了下一代RNA技术的过去、现状和未来。
01、环状RNA赛道梳理
1.1 环状RNA的发展
1976年,Sanger首先在植物类病毒中发现真核细胞的细胞质中存在环状RNA分子。 1993年,Capel发现小鼠Sry (sex-determining region Y)基因的环状RNA可能在小鼠睾丸发挥特定功能。 2013年,得益于高通量测序技术的发展,环状RNA被大量发现。Nature杂志同一期刊登两篇环状RNA研究文章,自此相关研究快速增长,逐渐成为RNA领域新的明星分子。

截止到目前,环状RNA发现已有40余年,近两年,全球环状RNA研究热情再上新高度。2021年,环状RNA领域实现近40亿元的融资规模,引起广泛关注。2021年环状RNA领域部分融资事件(资料来源:PharmaInvest数据库)
1.2 技术应用
环状RNA的特殊之处在于其结构。与以 5' 帽和 3' 尾终止的线性 RNA 不同,环状RNA 相当于线性 RNA 分子中的 3’ 和 5’ 端被连接形成了闭合环状结构,失去了 PolyA 尾巴。 这使得环状RNA能够抵御细胞内核酸酶的降解,提高RNA的表达时间和表达量,因此更为稳定,免疫原性也更低。 环状RNA具有重要的生物学功能,参与多种疾病的发生、发展过程。例如作为天然小RNA(miRNA)海绵体吸附并调控miRNA的活性,与转录调控元件结合或与蛋白互作调控基因的转录等。 已有研究表明,环状RNA与糖尿病、神经系统疾病、心血管疾病和癌症等疾病相关。环状RNA的广泛表达和疾病调控机制不仅有望成为这些疾病的临床诊断生物标志物,也可以作为疫苗和治疗手段。
1.3 行业优势
相较于线性mRNA,环状 RNA 技术相当于 mRNA2.0,在生产、递送和治疗效果方面更具有优势。环状RNA最大的潜力是能实现mRNA无法实现的药物需求。因环状RNA独特的构象,其在生物体内非常稳定,故其能够长时间的持续表达蛋白。 此外,环状RNA免疫原性也更低,不需要核苷酸修饰来避免先天性免疫应答,与未修饰的线性mRNA相比,纯化的未修饰的环状RNA可避免诱发 TLR/RIG-I介导的免疫反应。 凭借高稳定性和低免疫原性这两大特点,环状RNA能够延长给药频率,比mRNA更适合于长效性的RNA疗法开发。 环形RNA还能够通过设计与优化来实现在特定组织的高效表达,对药物的副作用形成巨大助力。这意味着,即便进入非目的的细胞组织,特异性表达也能够降低环形RNA在其他细胞中产生的副作用。 另一方面,环状RNA的制备工艺更加简单、递送更加灵活、生产和运输保存成本更低,因此产业化优势更加明显,是下一代新型药物开发的理想平台。
1.4 行业格局
如今,越来越多的创新企业便希望利用环状RNA的以上特点,超越mRNA技术。 Orna公司开发的基于环状RNA的CD19 CAR-T疗法已经进入临床阶段。由于该疗法直接体内产生经过修饰的免疫细胞,若临床成功无疑有望克服现有体外CAR-T 疗法制备周期长、成本高、安全性等障碍。 此外,该公司还布局了DMD管线,首次使用非病毒递送方式,将编码全长抗肌萎缩蛋白(dystrophin)的环形RNA递送到了人类细胞内部,并且表达抗肌萎缩蛋白,为DMD患者带来了希望。 在去年获得4.4亿美元高额融资的Laronde与Orna therapeutics的药物研发原理大致相同,均采用IRES(核糖体进入位点)技术激活eRNA翻译,但两者主要研究及应用方向存在一定差异。
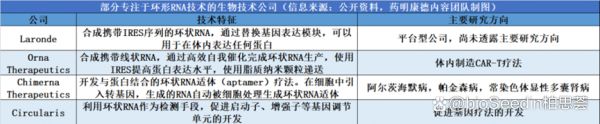
部分开发环状RNA的国外生物技术公司(信息来源:药明康德)
Laronde旨在通过AI的方法搭建eRNA药物研发及治疗平台。该公司的模块式环形RNA设计让它可以通过替换需要表达的转基因模块,让环形RNA表达任何类型的蛋白。
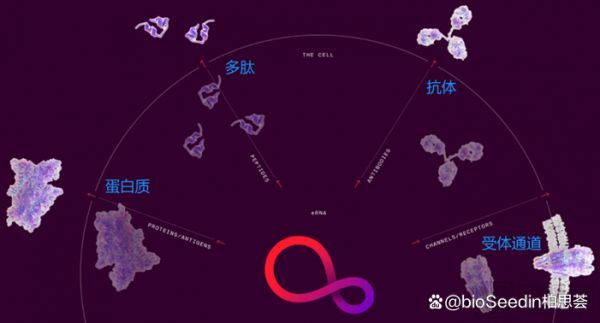
eRNA的“蛋白编码盒”(图片来源:Laronde)
国内企业也在前进。目前,以环码生物、圆因生物、吉赛生物、科锐迈德为代表的环状RNA新锐先后成立,纷纷打造了环状RNA技术平台,与海外企业齐头并进。
02、tRNA赛道梳理
2.1 概念和发展 转运 RNA(tRNA)是一类小的非编码 RNA,也是mRNA翻译过程中的一种辅助性分子。其最初被发现在蛋白质合成过程中充当氨基酸 “临时载体”,负责将其输送至生长中的多肽链末端。 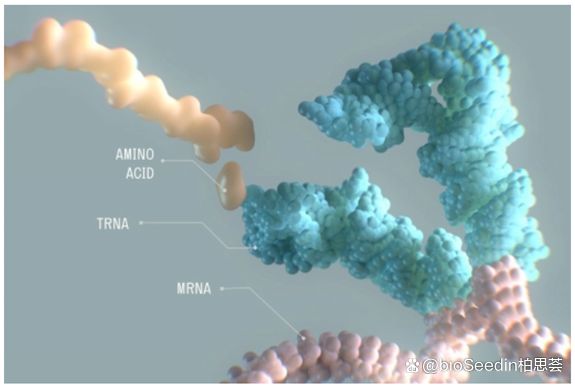
图片来源:ahotor.com
1965 年,tRNA 首次得到分离鉴定。tRNA 分子的二级折叠结构形似三叶草,其中包含反密码子(anticodon)序列和携带氨基酸的 3' 端。
1982年,来自加州大学旧金山分校的研究人员发现,一种能够读取过早终止密码子 (PTC)的人类tRNA可以帮助青蛙卵恢复全长蛋白质的生产。
随后几年,科罗拉多大学的研究人员在转基因小鼠身上验证了这种方法;此外,也有研究小组使用突变的抑制性tRNA在肌肉萎缩症小鼠模型中实现了低水平的疾病矫正。
2014年,葡萄牙癌症遗传学家Carla Oliveira领导的研究小组发现,抑制性tRNA具有治疗或预防无义突变引起的遗传性癌症综合症的潜力。
无义突变,即蛋白编码序列中有义密码子变为PTC的DNA突变,引发了大约11%的人类遗传病。目前基于tRNA疗法主要应用于罕见疾病领域中。
针对无意义突变主要有两种治疗方式。
一是对抑制性tRNA进行工程性编辑,使之能与内源性氨酰tRNA合成酶结合,让对应氨基酸结合上去,形成氨酰tRNA,在PTC的位置上,引入正常蛋白质对应的氨基酸,形成序列及全长都准确的正常蛋白质(图D)。
二是采用工程性无意义抑制性tRNA。与内源性氨酰tRNA合成酶结合,结合对应氨基酸,形成氨酰tRNA,在PTC的位置上,形成正常蛋白质(图B)。
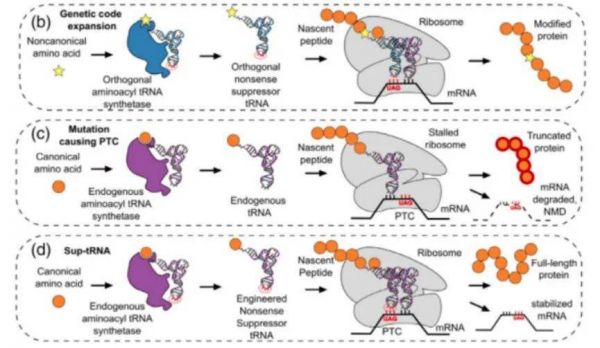
抑制性tRNA如何在疾病治疗中发挥作用(来源:WIREs RNA)
2.2 行业优势
相比基因疗法、mRNA疗法等,tRNA疗法有两个方面明显优势:首先,基于抑制性tRNA的治疗对于同一种类型的无义突变,具有通用性,对于过早终止密码子(PTC)是普遍适用的。 举个例子,对于编码谷氨酰胺的密码子CAG突变成TAG,导致无义突变造成的蛋白翻译终止,我们可以用一种携带谷氨酰胺并且识别提前终止密码子TAG的工程化tRNA,就能尝试治疗CAG无义突变导致的近三千种单基因遗传病。 其次,从大小来看,tRNA疗法的递送可能会更为灵活。tRNA本身很小,因此在递送方面不会遇到像利用病毒递送某些完整基因或者CRISPR酶一样的尺寸限制。 除此之外,抑制性tRNA的另一潜在优势是,在修复蛋白活性的同时不会引发蛋白过表达,这很重要,因为一些蛋白的过表达会引发新的问题。例如对于Rett 综合征患者,如果靶蛋白过表达可能会神经元产生毒性。 2.3 行业格局
tRNA是RNA疗法领域的融资“新星”。国际市场中,以ReCode Therapeutics、Shape Therapeutics和 Tevard Biosciences三家初创公司为首,斩获近 4 亿美元用于开发基于 tRNA 的疗法。此外,还有去年11月完成5000万美元种子轮融资的Alltrna,以及今年2月以2400万美元的A轮融资从隐形模式中脱颖而出的hC Bioscience。 Alltrna与hC Bioscience目前专注于tRNA疗法的开发,其他公司还布局了mRNA、RNA编辑等管线。 hC Bioscience正在推进两个互补平台,计划用 tRNA 对抗癌症和罕见疾病。PTCX平台同样利用了工程化tRNA识别mRNA转录本中的无义突变,通过插入一个氨基酸来抑制这种错误,从而保证正确的全长蛋白的产生。第二个基于tRNA的平台SWTX,则针对由不需要的蛋白质引起的疾病。该技术通过标记引起疾病的蛋白质,随后根据这个标记摧毁疾病的蛋白质。
Alltrna旨在利用AI设计靶向mRNA突变的tRNA,然后将合适的氨基酸转移到核糖体,从而能恢复正常蛋白质的生产。Alltrna开发的tRNA药物具有可编程性,未来将应用机器学习算法释放tRNA的治疗潜力。
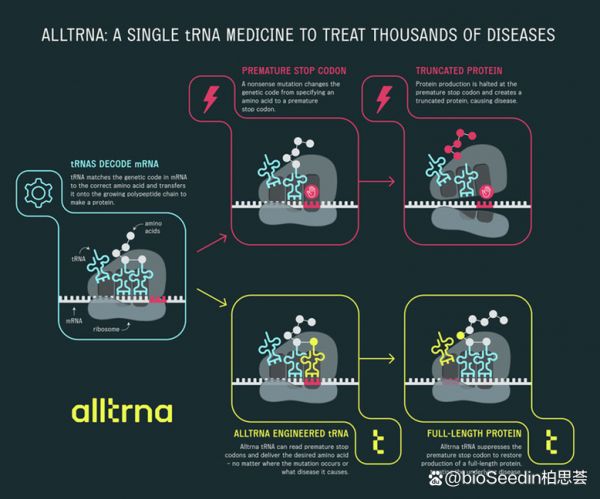
图片来源:Alltrna
在它们之前出现的ReCode Therapeutics、Shape Therapeutics 和 Tevard Biosciences也都在tRNA领域有了一定成果。 罗氏在去年8月与Shape Therapeutics公司达成超30亿美元的研发合作。与Alltrna的技术原理类似,Shape公司的RNAskip技术平台也是通过设计独特的tRNA识别RNA序列上过早出现的终止密码子,让转移过程能够通读这些密码子,生成正常的蛋白。Shape正在开发治疗Rett综合征的抑制性tRNA,该疾病是一种神经发育障碍,由MECP2基因的无义突变导致。 Tevard的目标是利用tRNA作为Dravet综合征和其它PTC相关疾病的基因治疗替代疗法。ReCode Therapeutics则采用了LNP将tRNA分子递送到靶细胞中进行疾病的治疗,其治疗囊性纤维化的tRNA药物有望在今年达到IND阶段。 国内方面,由夏青教授创办的启夏解码(QiXia Decode Therapeutics)正在专注于利用工程化tRNA–酶(tRNA–enzyme pairs)治疗无义突变引起的肌肉营养不良和癌症,该公司于2021年成立,迄今为止已经筹集了1600万美元。
小结 新冠疫情给mRNA的发展助推了一把,并延伸到其他RNA领域,给行业带来了新风口。环状RNA和tRNA自发现以来已有40余年,Alltrna、Laronde等公司由知名风投机构Flagship Pioneering孵化建立,该领域也受到了默沙东、罗氏等制药巨头的看好,可能意味着下一代RNA相关疗法的曙光已现。
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
“元气”泄气 健康饮料新赛道还没起飞就变“泡沫”?
人形机器人泡沫要破?朱啸虎看不清商业路径喊撤退,创投圈炸锅
积极拥抱产业变革新机遇 ——浅谈 2024 年医疗健康产业投资策略
无糖气泡水赛道,究竟有没有泡沫?
2024大健康投资解析:市场回暖,创新药与器械赛道机遇多
2023上半年营养健康产业投融资洞察,哪些赛道更“吸金”?
资本巨头2000亿元下注大健康 业内人士直呼“疯狂”
“中年发福”90后为之疯狂的轻食代餐!背后是千亿市场还是一场泡沫?
健康食品产业 市场欣欣向荣资本翩翩起舞
21创投行研|知名机构纷纷入局,心理健康赛道创业投资机会如何?
网址: 下一代RNA赛道:资本泡沫还是产业机遇? https://m.trfsz.com/newsview1551152.html

