【重磅】中医药真实世界研究的标准化建设“由下而上”渐入佳境!
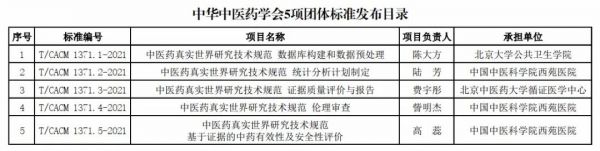
中医药真实世界研究系列技术规范的制定,旨在针对真实世界数据应用的不同环节,建立科学合理的技术规范和评价原则。1.《中医药真实世界研究技术规范 数据库构建和数据预处理》(项目负责人:陈大方;承担单位:北京大学公共卫生学院)近年来,真实世界数据产生的相关证据在中药新药研发中的重要性日益凸显,在数据规范化、多源信息整合和安全隐私保护等方面需要制定统一、可参照的标准。中医药真实世界研究技术规范之数据库构建和数据预处理是遵照开展真实世界研究获得真实世界证据的基本原则而制定的基本规范,是中医药真实世界数据开展真实世界研究系列技术规范之一,本规范基于中医药真实世界数据特点,结合《真实世界证据支持药物研发与审评的指导原则(试行)》和《用于产生真实世界证据的真实世界数据指导原则(试行)》等技术文件对真实世界数据的要求,明确了数据库构建和数据预处理的技术规范,以保证中医药真实世界研究结果的真实性和可靠性,提高中医药真实世界研究质量。(此部分内容由项目组提供)
 2.《中医药真实世界研究技术规范 统计分析计划制定》(项目负责人:陆 芳;承担单位:中国中医科学院西苑医院) 应用真实世界数据科学评价中医药的有效性与安全性较之严谨设计的随机对照临床试验面临的数据处理和统计分析更复杂,需要对研究的相关因素作出合理、有效的安排,最大限度地控制混杂与偏倚,并对研究结果进行科学的分析和合理的解释, 形成严谨完整的证据链,达到与传统临床试验证据互为补充的目的。本规范在参照《真实世界证据支持药物研发与审评的指导原则(试行)》、《药物临床试验的生物统计学指导原则》等相关法律法规和技术文件指导的框架下,提出应用真实世界数据制定统计分析计划的一般要求,从研究设计、统计分析方法、分析内容等方面进行详细的规范制定,以指导应用真实世界数据进行中药研发和中医药临床科研的统计分析工作。(此部分内容由项目组提供)
2.《中医药真实世界研究技术规范 统计分析计划制定》(项目负责人:陆 芳;承担单位:中国中医科学院西苑医院) 应用真实世界数据科学评价中医药的有效性与安全性较之严谨设计的随机对照临床试验面临的数据处理和统计分析更复杂,需要对研究的相关因素作出合理、有效的安排,最大限度地控制混杂与偏倚,并对研究结果进行科学的分析和合理的解释, 形成严谨完整的证据链,达到与传统临床试验证据互为补充的目的。本规范在参照《真实世界证据支持药物研发与审评的指导原则(试行)》、《药物临床试验的生物统计学指导原则》等相关法律法规和技术文件指导的框架下,提出应用真实世界数据制定统计分析计划的一般要求,从研究设计、统计分析方法、分析内容等方面进行详细的规范制定,以指导应用真实世界数据进行中药研发和中医药临床科研的统计分析工作。(此部分内容由项目组提供) 3.《中医药真实世界研究技术规范 证据质量评价与报告》(项目负责人:费宇彤;承担单位:北京中医药大学循证医学中心)近年来,真实世界数据产生的相关证据在中药新药研发中的重要性日益凸显。真实世界证据的质量直接影响着证据的科学性、真实性、适用性等,对临床决策具有重要意义。然而目前真实世界研究质量评价方面尚缺乏统一标准。《中医药真实世界研究技术规范证据质量评价与报告》旨在为真实世界证据在中药新药研究中的应用定位和合理使用形成指导。本文件适用于中药新药研发工作中真实世界证据质量评价及规范报告的参考,亦可作为医疗机构、中药研发企业、中医药科研机构的人员对各类中医药临床研究证据的质量评价。主要内容包括:真实世界研究设计分类、真实世界证据、真实世界证据的质量评价的总体原则与方法、真实世界研究常见偏倚、评价中医药真实世界证据质量的特殊考虑、不同类型真实世界证据质量的具体评价方法,真实世界证据的报告规范,以及真实世界证据分级。(此部分内容由项目组提供)
3.《中医药真实世界研究技术规范 证据质量评价与报告》(项目负责人:费宇彤;承担单位:北京中医药大学循证医学中心)近年来,真实世界数据产生的相关证据在中药新药研发中的重要性日益凸显。真实世界证据的质量直接影响着证据的科学性、真实性、适用性等,对临床决策具有重要意义。然而目前真实世界研究质量评价方面尚缺乏统一标准。《中医药真实世界研究技术规范证据质量评价与报告》旨在为真实世界证据在中药新药研究中的应用定位和合理使用形成指导。本文件适用于中药新药研发工作中真实世界证据质量评价及规范报告的参考,亦可作为医疗机构、中药研发企业、中医药科研机构的人员对各类中医药临床研究证据的质量评价。主要内容包括:真实世界研究设计分类、真实世界证据、真实世界证据的质量评价的总体原则与方法、真实世界研究常见偏倚、评价中医药真实世界证据质量的特殊考虑、不同类型真实世界证据质量的具体评价方法,真实世界证据的报告规范,以及真实世界证据分级。(此部分内容由项目组提供)  4.《中医药真实世界研究技术规范 伦理审查》(项目负责人:訾明杰;承担单位:中国中医科学院西苑医院)利用已有的、正在产生的、将要形成的真实世界数据并对这些证据进行评价后应用于中药有效性和安全性评价,应注意每种情况下因不同的设计涉及不同环节的伦理问题,应遵循一定的伦理审查技术规范。伦理审查对于所有涉及人的生物医学研究都具有普适性,但在真实世界数据用于临床研究时,又面临着独特的挑战:数据产生的前提、数据提取所涉及的伦理问题、数据转移和存贮应注意的伦理问题、数据的反馈、数据共享及发表时所涉及的伦理问题。本规范旨在建立将真实世界数据应用于中医药临床研究,从而形成真实世界证据用于支持药物研发和审评过程中,各环节涉及的伦理问题的审查技术规范,为数据应用于临床研究从而转化为证据使用的过程符合科学性、伦理性提供技术参考。(此部分内容由项目组提供)
4.《中医药真实世界研究技术规范 伦理审查》(项目负责人:訾明杰;承担单位:中国中医科学院西苑医院)利用已有的、正在产生的、将要形成的真实世界数据并对这些证据进行评价后应用于中药有效性和安全性评价,应注意每种情况下因不同的设计涉及不同环节的伦理问题,应遵循一定的伦理审查技术规范。伦理审查对于所有涉及人的生物医学研究都具有普适性,但在真实世界数据用于临床研究时,又面临着独特的挑战:数据产生的前提、数据提取所涉及的伦理问题、数据转移和存贮应注意的伦理问题、数据的反馈、数据共享及发表时所涉及的伦理问题。本规范旨在建立将真实世界数据应用于中医药临床研究,从而形成真实世界证据用于支持药物研发和审评过程中,各环节涉及的伦理问题的审查技术规范,为数据应用于临床研究从而转化为证据使用的过程符合科学性、伦理性提供技术参考。(此部分内容由项目组提供)  5.《中医药真实世界研究技术规范 基于证据的中药有效性及安全性评价》(项目负责人:高 蕊;承担单位:中国中医科学院西苑医院)真实世界临床研究的有效性及安全性评价,是遵照循证医学的理念、基于系列真实世界研究的证据,探索干预措施在实际临床诊疗状况下,体现患者受益的临床症状、实验室指标、终点事件、生活质量等指标的变化,是临床评价领域重要组成。近年来,真实世界数据产生的相关证据在中药新药研发中的重要性日益凸显,本规范参考《真实世界证据支持药物研发与审评的指导原则(试行)》人用数据支持药物研发的相关要求,旨在建立利用真实世界证据对药物的有效性及安全性进行评价的技术规范,指导对拟研究品种的人用经验产生的研究证据进行有效性评价、安全性评价,用于指导中药新药和院内制剂的研发。(此部分内容由项目组提供)
5.《中医药真实世界研究技术规范 基于证据的中药有效性及安全性评价》(项目负责人:高 蕊;承担单位:中国中医科学院西苑医院)真实世界临床研究的有效性及安全性评价,是遵照循证医学的理念、基于系列真实世界研究的证据,探索干预措施在实际临床诊疗状况下,体现患者受益的临床症状、实验室指标、终点事件、生活质量等指标的变化,是临床评价领域重要组成。近年来,真实世界数据产生的相关证据在中药新药研发中的重要性日益凸显,本规范参考《真实世界证据支持药物研发与审评的指导原则(试行)》人用数据支持药物研发的相关要求,旨在建立利用真实世界证据对药物的有效性及安全性进行评价的技术规范,指导对拟研究品种的人用经验产生的研究证据进行有效性评价、安全性评价,用于指导中药新药和院内制剂的研发。(此部分内容由项目组提供)  标准化办公室发布中华中医药学会 标准化办公室 电话:010-64205923 64202516 微信:中医药标准化 地址:北京市朝阳区樱花园东街甲4号 邮箱:bzhtcm@163.com
标准化办公室发布中华中医药学会 标准化办公室 电话:010-64205923 64202516 微信:中医药标准化 地址:北京市朝阳区樱花园东街甲4号 邮箱:bzhtcm@163.com 
【声明】
推送此文是出于传递更多信息之目的。若参考文章和文献中有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本号联系,我们将及时更正、删除,谢谢!邮箱地址:409426501@qq.com本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
关键词:
中医药,标准化,建设,研究,数据,伦理,技术,中药
相关知识
从“纸上”到“云上”,大数据重构真实世界医学研究体系
大批药企,开展真实世界研究
行业革新!保健食品真实世界研究与标准化的融合之道
2025年保健食品行业资讯:真实世界研究标准发布推动行业科学化进程
健康之路通过上市聆讯,真实世界研究年收入超4亿、新增长点浮现
临床研究方法中的比较效果研究、实效研究和真实世界研究是什么
什么是真实世界研究?真实世界研究和随机对照临床试验有何区别?
实效性随机对照试验:提供来自真实世界研究的证据
藿香正气液启动“真实世界研究” 推动传统中药研究升级转型
中药标准国际化的拓荒之旅——记中科院上海药物研究所中药现代化研究团队
网址: 【重磅】中医药真实世界研究的标准化建设“由下而上”渐入佳境! https://m.trfsz.com/newsview1577810.html