氟比洛芬凝胶贴膏人体生物等效性研究分析

作者 | 肖凡
校对 | 马科强
一、背景骨性关节炎(骨关节炎,OA),也称退行性关节炎,是一种常见的慢性、退行性骨关节疾病。该病好发于中老年人,常导致关节疼痛、僵硬和活动受限,致残率较高,给家庭和社会带来沉重的精神和经济负担[1]。其中膝骨关节炎是一种病因机制尚未完全明确的骨科常见病、多发病,严重影响患者的生活质量,女性患病的概率是男性患病概率的2.46倍;年龄每增长1岁,膝骨关节炎的患病率就会提升1.05倍[2]。与骨关节炎有关的风险因素有遗传、BMI、生活方式、营养、性激素、生殖、骨密度、机械因素、外伤、体力活动、肌肉力量、职业等[3]。
在治疗整形外科领域各种疼痛性、炎症性疾病时,主要口服非甾体性镇痛、消炎剂并取得了显著的效果。氟比洛芬是具有强力的前列腺素合成抑制作用的苯基丙酸系的非甾体性镇痛消炎剂,以往作为口服剂广泛用于以整形外科领域为首的各种疼痛性疾病。但是,一般非甾体性镇痛消炎剂,通过内服,有较为明显的胃肠系统不良反应,患者口服给药的依从性并不良好[4]。近些年,应用于镇痛领域的经皮给药系统的药物发展迅猛,经皮给药系统相较于口服、注射等给药方式具有许多优势:①避免肝脏的首过效应;②药物吸收不受胃肠道内pH值、食物及其他药物等因素的影响;③具有控释效果;④维持恒定的有效血药浓度,避免因吸收过快产生血药浓度过高引起不良反应;⑤给药方便,安全性高,患者顺应性好。事实证明,该技术可以成功替代各种侵入式给药方式[5]。氟比洛芬凝胶贴膏作为经皮给药贴剂,能够发挥对炎症局部的直接效果,并且抑制药物的血药浓度,减轻全身性副作用,同时能够提供持续的效果,适用于治疗骨关节炎、肩周炎、肌腱及腱鞘炎、腱鞘周围炎、肱骨外上髁炎(网球肘)、肌肉痛、外伤所致肿胀、疼痛。氟比洛芬凝胶贴膏(商品名:Zepolas®/ゼポラス®)是由日本三笠制药株式会社率先研发,包含两种规格:40 mg/贴和80 mg/贴,分别于1988年5月和2009年7月在日本批准上市,其中,40 mg/贴以原研进口、国内分包的形式于2019年在我国上市,商品名为泽普思®。
本文将结合相关指导原则和文献研究,详细阐述氟比洛芬凝胶贴膏临床研究的一般考虑,对本品人体生物等效性研究的若干关键设计进行探讨,旨在为此类产品的仿制和注册申报提供参考。
二、品种基本情况 通用名称:氟比洛芬凝胶贴膏(曾用名:氟比洛芬巴布膏) 商品名称:泽普思® 英文名称:Flurbiprofen Cataplasms 化学结构式: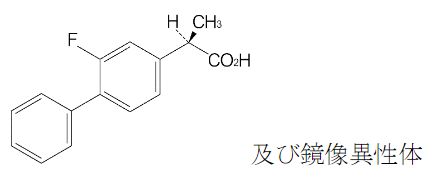
1、研究类型
根据《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则》,生物等效性研究方法按照研究方法评价效力,其优先顺序为药代动力学研究、药效动力学研究、临床研究和体外研究。氟比洛芬凝胶贴膏经皮给药发挥全身作用,其活性成分氟比洛芬在体内的血药浓度可以准确定量,因此本品生物等效性研究推荐开展一项在健康受试者体内进行的PK-BE研究。2、受试者选择
健康受试者是较为理想的皮肤条件均质性的受试人群,能更好的反映出受试制剂与原研药之间的PK差异,因此一般推荐健康男性和女性受试者。需根据剂型特点排除有皮肤病史者或已知可改变皮肤外观或生理反应病史者,身体拟用药的对称部位肤色有明显差异、应用部位有疤痕组织、纹身等影响药物粘贴、吸收以及皮肤状态评估的受试者也应排除。3、给药剂量与给药方式
建议选用已在国内上市的原研氟比洛芬凝胶贴膏作为参比制剂(规格:40 mg,13.6cm×10.0cm),于每名受试者的背部干燥清洁的完整皮肤上贴敷1贴受试制剂或参比制剂,用手掌压至少20~30 s保证贴膏完全黏附,持续用药12 h后移除贴膏。给药前保证给药部位皮肤清洁干燥,多余的毛发需进行修剪,不能涂沫护肤品、酒精等。用药期间,受试者应避免任何可能导致出汗及降低贴剂黏附性的剧烈运动,不允许有任何形式的挤压给药部位的姿势,受试者避免擦、拉或触摸贴剂,以及避免进行任何可能导致贴剂移位的活动,也不要用外物覆盖或者遮住贴膏。4、血样采集
原研资料中氟比洛芬凝胶贴膏的药代动力学参数[4]如下:
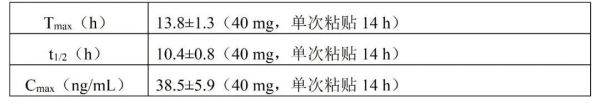
5、黏附性评价
FDA于2018年10月发布了《Assessing Adhesion With Transdermal and Topical Delivery Systems for ANDAs Guidance for Industry》[6](ANDA所需的透皮递药系统和外用贴剂黏附力评估)指导原则,对于透皮贴剂的黏附力评价进行了规定,申请人需通过五点黏附量表进行分值(0-4分)对受试制剂和参比制剂各自的黏附力进行评估,其中黏附量表如下: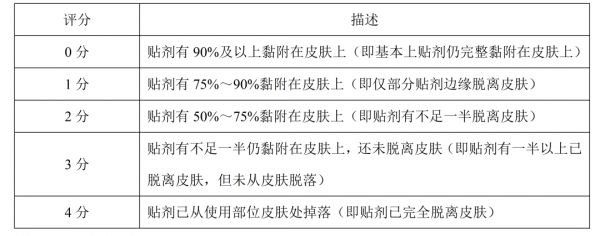
6、皮肤刺激性和致敏性评价
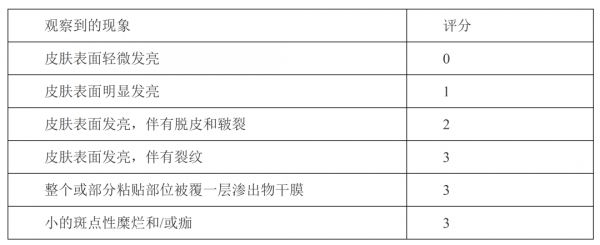
同样为了规范申请人在透皮和皮肤外用制剂开发过程中对于皮肤刺激性和致敏性的研究,FDA于2018年10月发布了《Assessing the Irritation and Sensitization Potential of Transdermal and Topical Delivery Systems for ANDAs》[7](ANDA透皮和局部给药系统的刺激和致敏潜力)指导原则,对于皮肤刺激性和致敏性评价研究的开展提供了特殊规定,针对透皮贴剂,申请人需在移去贴片后若干时间点观察贴剂使用部位皮肤刺激性情况并进行彩色拍照,此后由2个独立的观察人员根据皮肤刺激性评估标准评估,并记录评分。皮肤刺激性评分标准如下:1)皮肤反应
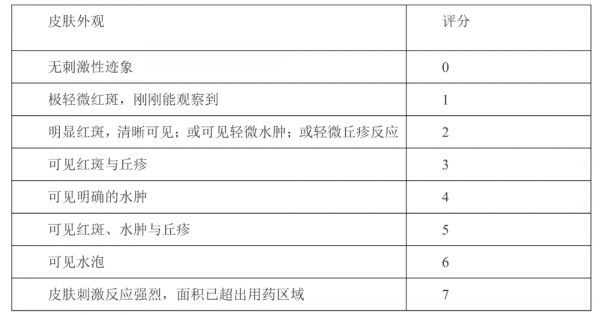
2)其他皮肤反应
7、国内申报情况分析
氟比洛芬凝胶贴膏原研产品40 mg(13.6cm×10.0cm)的贴膏于2016年获准在我国上市,目前国内仅有北京泰德制药一家获批该品种仿制药,之前以新四类申报的湖南九典和哈尔滨三联药物均未获得批准,目前按照化药4类申报生产的企业包括乐明药业、武汉法玛星制药等在内,同时该品种在CDE有多个申请人登记了生物等效性试验,竞争可谓非常激烈。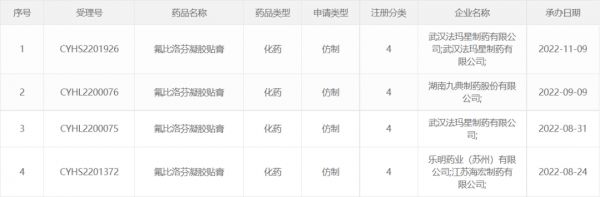
图源 CDE在审评品种目录
四、总结
有研究表明,氟比洛芬凝胶贴膏的镇痛效果与口服同等剂量氟比洛芬在几乎相当的情况下,贴膏剂还具有使用便利、快速起效、局部浓度高等特点,同时凝胶质地皮肤相容性以及渗透性好,多重优点使其在镇痛大领域中具有广阔的应用市场。但作为一种经皮给药制剂,该品种的仿制药研发和临床评价均具有较高的技术门槛,给众多布局该品种的企业带来了挑战。
本文总结了氟比洛芬凝胶贴膏生物等效性研究的现状,结合现有相关技术指南,期望为氟比洛芬凝胶贴膏仿制药研发BE试验的技术攻关提供有价值的参考。我司致力于帮助众多申办者进行复杂项目的临床评价。其中,在皮肤外用制剂如乳/软膏、凝胶、透皮给药等外用制剂的BE研究领域积累了丰富的经验,已完成包括银离子抗菌功能性敷料、黄体酮阴道缓释凝胶、罗替高汀贴片、利丙双卡因乳膏等在内的多个外用制剂BE研究,成功助力多家药企完成上述品种的申报。
五、参考文献
[1]陈泓伯,吴俊慧,武轶群,王紫荆,吴瑶,吴涛,王梦莹,王斯悦,王小文,王伽婷,于欢,胡永华.2015-2017年北京市成年骨关节炎患者主要合并症的流行病学研究[J].第三军医大学学报,2021,43(12):1103-1108.
[2]黎丹东,李琳琳,苏峰,张旭辉,郭广惠,马珍珍.膝骨关节炎与性别和年龄的相关性研究[J].临床医学研究与实践,2019,4(31):1-3+8.
[3]Update on the epidemiology, risk factors and disease outcomes of osteoarthritis
[4]氟比洛芬凝胶贴膏原研IF文件
[5]韩佳琦,刘哲鹏.经皮给药系统的研究进展[J].生物医学工程学进展,2022,43(01):24-28.
[6]Assessing Adhesion With Transdermal and Topical Delivery Systems for ANDAs Guidance for Industry
[7]Assessing the Irritation and Sensitization Potential of Transdermal and Topical Delivery Systems for ANDAs Guidance for Industry
预知更多品种分析,请咨询↓↓↓

相关知识
氟比洛芬凝胶贴膏成分有什么
氟比洛芬凝胶贴膏有什么可以替代
氟比洛芬凝胶贴膏(泽普思)能长期使用吗?
孕妇能否使用氟比洛芬凝胶贴膏?
氟比洛芬凝胶贴膏的功效与作用是怎样的呢?
使用氟比洛芬凝胶贴膏多久为一疗程
孕妇可以使用氟比洛芬凝胶贴膏吗?
肠胃不好的人可以使用氟比洛芬凝胶贴膏的吗?
氟比洛芬凝胶贴膏(泽普思)是怎么样使用的呢?
氟比洛芬凝胶贴膏的副作用有吗?能长期使用吗?
网址: 氟比洛芬凝胶贴膏人体生物等效性研究分析 https://m.trfsz.com/newsview1754024.html