维生素 D 和钙补充剂与尿石症:一个有争议的多方面关系
Messa P, Castellano G, Vettoretti S, Alfieri CM, Giannese D, Panichi V, Cupisti A. Vitamin D and Calcium Supplementation and Urolithiasis: A Controversial and Multifaceted Relationship. Nutrients. 2023 Mar 31;15(7):1724. doi: 10.3390/nu15071724. PMID: 37049567; PMCID: PMC10096570.
一、简介
尿石症 (UL) 是世界上最常见的疾病之一,大约每 10-12 名普通人群中就有一人经历过一次 UL,男性的患病率大约是女性的两倍。这些受试者中有一半或更多在未经治疗的情况下,在其一生中至少经历过一次尿路结石复发。尿石症,特别是当复发和/或并发梗阻性肾病或感染时,可诱发肾损伤,可演变成慢性肾病 (CKD),最终,尽管在少数患者中,终末期肾病 (ESKD) [ 5 , 6 , 7 , 8 , 9 ]。此外,UL事件对患者的生活质量有重大影响,并与直接(与干预相关)和间接(工作日损失)的医疗保健成本显着增加有关。尽管 UL 的病因仍远未完全阐明,但据称遗传和环境因素都在不同程度上促成了肾结石形成的发生。
人们还普遍认识到,这一病理过程的主要致病机制与促进物质(例如钙、草酸盐、尿酸、胱氨酸、药物)和抑制物质(例如柠檬酸盐)的尿液浓度之间平衡的破坏有关,镁)尿路结石的形成过程。事实上,促进剂的增加和/或抑制剂的减少,通常与相对较低的尿量或氢离子浓度的变化有关,会增加泌尿环境中结晶形成的风险,这是尿结石发生的第一步。
尽管大多数尿路结石由多个分子组成,但到目前为止,钙盐是所有成分中最多的,因为大约 80%的尿路结石含有钙盐(主要是草酸钙,少量是磷酸钙). 此外,高钙尿症 (HC )是肾结石形成(SF) 受试者尿液中最常见的代谢异常。
2. 高钙尿症和尿石症
HC 和 UL 之间的联系源于大约一个世纪前的研究。1939 年,Flocks RH 报道了 SF 患者尿液中钙水平升高,支持尿钙浓度升高在 UL 发病机制中的直接作用 [ 22 ]。从那时起,人们对研究领域越来越感兴趣,以更好地定义 HC 的机制和致病因素,还提出了诊断方法,这些方法在临床医学的现实世界中很容易执行。
每日尿钙排泄水平的定义应被视为“正常”阈值,高于该阈值就可以对 HC 进行可靠诊断,这仍然是一个有争议和争论的问题 。由于目前手稿的性质,主要针对讨论一些临床实践方面,我们认为在这里讨论这个话题不合适。作为定义 HC 的实用阈值,我们决定采用每天摄入钙的饮食的受试者的尿钙参考水平大于 4 mg/Kg/d 或女性 250 mg 和男性 300 mg 1000-1200毫克的含量,代表一般人群钙摄入量的推荐值。
传统上,HC 分为三大类:肠道(或吸收性)HC;肾漏 HC;和骨吸收HC 。然而,上述 HC 类型之间存在明显的发病机制差异,甚至这种分类的临床相关性受到质疑。尽管这个主题可能具有重要的生理病理学和临床意义,但我们认为在本次讨论中深入讨论细节没有用,我们将自己局限于处理一些特殊方面,在我们看来,这些方面在相关方面具有更大的实际意义到本次审查的主要目的。
2.1. 小肠吸收碳氢化合物
钙从肠道进入体内池的增加可以通过两种不同的途径发生:第一种主要是继发于饮食来源和/或补充剂中钙摄入量的增加,这通过细胞旁扩散诱导肠道吸收增加主要由浓度梯度驱动的运输机制;第二种主要是由于钙通过肠细胞的跨细胞转移增加,通过高度依赖维生素 D 可用性和有效性的主动饱和转运机制。鉴于缺乏平衡研究,在通常的饮食摄入量下通过肠道途径吸收的钙净量的精确估计仍然只是模糊定义 [ 27 ]。然而,人们可以预期在其膳食含量的绝对量增加和/或由于活性维生素 D 代谢物的水平增加或对活性维生素 D 代谢物的敏感性增强而导致更活跃的肠道钙转运的情况下,肠道钙的净吸收增加. 然而,这两种不同类型的吸收性 HC 之间存在一些独特的差异,特别是在发展 UL 的相关风险方面,值得专门讨论。
首先,鉴于正常受试者在代谢平衡条件下通常吸收正常饮食中钙含量的 15-20%(800-1000 毫克钙),因此根据之前报道的实用定义,预计 HC只有当饮食中的钙含量超过 1200-1500 毫克时才能观察到。另一方面,如果一个人暴露于更高水平的维生素 D 和/或对维生素 D 活性的敏感性增加,通过主动吸收途径导致的钙吸收增加,即使饮食中含有钙含量,也可能导致 HC在推荐范围内甚至低于推荐范围。其次,对于每天引入的相同量的口服钙,与摄入钙后的净钙吸收相比,当主要通过进餐时食用富含钙的食物或饮料引入口服钙摄入时,吸收的钙量要低得多膳食补充剂或富含钙的饮料。这种差异是次要的,因为当与食物一起引入时钙被吸收的生物利用度降低。发生这种情况是因为钙离子可以与膳食阴离子结合,即磷酸盐、草酸盐、硫酸盐等。当从食物中摄取钙时,这种机制不起作用。这种差异与 UL 的风险密切相关,因为在进餐时增加钙摄入量也可能起到保护作用,因为草酸盐可能与肠道中的钙结合,图1和图 2). 事实上,几十年前,我们证明,从无钙饮食转向限钙饮食(400 毫克/天)的 SF 患者的尿液草酸盐排泄显着增加,尽管钙排泄减少,草酸钙的相对过饱和度几乎翻了一番 [ 28]. 在同一方向上,更具指示性的是 Curhan 及其合作者的数据,他们通过对两个没有 UL 病史的大型受试者队列进行的两项前瞻性观察研究清楚地表明,进餐时钙摄入量的增加与较低的UL 的发生率。相比之下,在随访期间,通过主要在餐外摄入的钙补充剂增加钙摄入量显然与更高的肾结石发病率相关[ 29、30 ]。
图1膳食外补钙对 UL 风险的潜在影响。在餐外服用钙补充剂时,吸收的钙量更多,因为钙不能与膳食阴离子(磷酸盐、草酸盐、硫酸盐等)结合,这为肠道吸收增加了钙和游离阴离子的量,导致钙、草酸盐和磷酸盐的尿液排泄增加。F-Ca : 过滤钙;PTH:甲状旁腺激素。
图 2随餐补充钙对 UL 风险的潜在影响。随餐服用钙补充剂时,钙会与膳食阴离子(磷酸盐、草酸盐、硫酸盐等)结合,从而减少钙本身和相关阴离子的吸收。在正常的膳食钙摄入量范围内(800-1000 毫克)并且维生素 D 水平没有升高,这甚至可以转化为降低尿路结石风险。F-Ca : 过滤钙;PTH:甲状旁腺激素。
最后,与维生素 D 活性增加相关的 HC(由于水平增加和/或对其作用的敏感性增加)可能对形成尿路结石的风险产生更相关的影响。事实上,维生素 D 不仅能增强肠道钙的主动转运,即使钙摄入量在正常范围内也能诱导 HC,而且,由于维生素 D 介导的钙转运增强主要发生在近端胃肠道,较少量的钙到达远端肠道。由于它是草酸盐吸收的主要部位,与钙结合的草酸盐减少,导致肠道吸收增加,从而增加草酸盐的尿排泄。此外,维生素 D 活性增加会导致甲状旁腺激素 (PTH) 减少,骨细胞产生和分泌成纤维细胞生长因子 23 (FGF-23) 增加,从而分别导致远端和近端肾脏的钙和磷酸盐重吸收减少肾小管水平,这反过来又导致钙和磷酸盐的尿液排泄增加。总体最终效果是草酸钙和磷酸钙的相对过饱和度增加,导致钙 UL 的风险增加(图 3).
图 3补充维生素 D 对 UL 风险的潜在影响。维生素 D 刺激钙的主动转运,主要是在近端肠道,即使钙摄入量在正常范围内也会诱导 HC;由于较少的钙到达远端肠道,更多的草酸盐仍然游离在远端肠道中被吸收;维生素 D 还可以抑制 PTH 的产生并刺激骨细胞产生 FGF-23,从而分别减少肾小管对钙和磷酸盐的重吸收。所有这些影响都转化为草酸钙和磷酸钙相对尿液过饱和度的增加。FGF-23:成纤维细胞生长因子 23;F-Ca : 过滤钙;HC : 高钙尿症; 甲状旁腺素: 甲状旁腺激素。
2.2. 骨吸收 HC
传统上,继发于骨吸收增加的 HC 的原型形式与 PTH 分泌的原发性增加(即原发性甲状旁腺功能亢进症,PHP)相关,其中尿钙排泄增加是由于血清钙增加导致滤过钙增加由 PTH 直接刺激的骨吸收增加和由 PTH 诱导的骨化三醇水平增加继发的肠钙吸收增加引起的浓度。较高的血清钙水平会导致肾小球滤过钙增加,这会超过肾小管钙转运能力,尽管会因 PTH 的作用而增强,并最终导致 HC,这会导致 PHP 患者 UL 的发病率增加 [31 ]]. 事实上,这种形式的 HC 属于混合型,因为吸收(肠道)和再吸收(骨骼)成分均有助于其发生。
事实上,一种不依赖 PTH 的骨吸收增加形式已被认为是尿路结石患者 HC 的常见原因。这种形式的 HC 通常以高水平的空腹尿钙排泄(空腹 HC)为特征,并且与钙丢失形式的 HC 有许多相似之处,将在下一节中更详细地讨论。
2.3. 肾漏 HC
肾小管钙泄漏,即所谓的肾 HC,长期以来一直被认为是 HC 的第二大最常见原因,仅次于肠道 HC [ 32、33 ]。以前,肾 HC 的定义是空腹尿液中钙排泄增加(空腹 HC)、血清钙浓度正常至低水平以及甲状旁腺激素 (PTH) 水平正常至高水平。所有这些特征都非常适合继发性甲状旁腺功能亢进症 (SHP) 作为肾脏钙流失的补偿机制[ 34、35 ]。除了罕见形式的涉及肾小管钙转运的遗传缺陷 [ 12 , 36 , 37],随后的研究无法证实任何类型的肾小管钙转运缺陷的明显存在,更不用说 SF 受试者中与空腹 HC 相关的 SHP 的存在,这表明骨吸收的 PTH 非依赖性增加可能是禁食期间尿钙排泄增加的潜在机制 。在假设的发病机制中解释与禁食 HC 相关的 PTH 非依赖性骨吸收增加,一些作者提出,一些单核细胞衍生细胞因子的产生增加可能与破骨细胞活化有关,随之而来的是矿物质骨吸收的增加 。
也有人提出,食用富含动物蛋白的饮食(主要由于硫酸盐含量而导致酸负荷增加)可以直接增加骨吸收,这是由于氢离子对破骨细胞活性的刺激作用 。_ 此外,据报道,动物蛋白摄入量的增加会导致前列腺素 E-2 (PGE-2) 的产量增加,而 PGE-2 也是骨吸收机制的有效刺激物。
其他作者提出了一些钙传感器受体 (CaSR) 多态性变体的作用,以解释 PTH 非依赖性空腹 HC 的发病机制 [ 51 ]。过去,当 CaSR 首次被发现和表征时 [ 52 ],它被描述为一种 G 蛋白偶联受体,在甲状旁腺细胞上表达,主要作为细胞外钙水平的专门传感器,其激活由钙浓度能有效抑制PTH的分泌和合成。然而,很快人们就意识到 CaSR 也被除甲状旁腺以外的许多组织中的几种细胞表达,包括肾小管细胞,其激活后钙摄取减少,从而增加尿液排泄 [53 , 54 ]。由于所描述的 CaSR 多态性变体 [ 51 ] 的特点是受体功能的增加,作者假设它可能是参与 SF 患者 PTH 非依赖性空腹 HC 发病机制的一个因素,其中这种多态性的发生率高于非 SF 科目。
其他遗传因素,如可溶性腺苷酸环化酶基因 (ADCY10) 或密蛋白 14 基因 (CLDN14) 的多态性,也被认为在 SF 患者观察到的骨丢失中发挥致病作用。除了所有这些可能的因素之外,还经常添加一种错误的信念,即建议所有尿路结石患者,尤其是 HC 患者遵循减少摄入含钙食物的饮食是适当且有用的。
尽管这一信念已被科学研究的结果明确否定,但它仍然存在于世界许多地区的流行文化中,导致缺钙的情况,这远非有助于抵消结石病过程,肯定有助于以减少骨量。
无论如何,无论空腹尿钙排泄增加的致病机制是什么,无论是否依赖 PTH,许多研究报告说,HC,尤其是空腹型 HC,通常与骨矿物质含量降低和风险增加有关骨折。
3. 一般人群补充维生素 D 和/或钙的适应症
骨骼骨折是普通人群的主要健康和社会问题之一,低骨量,特别是骨质疏松程度,是导致和诱发骨骼骨折的主要因素之一。最近的研究报告称,根据世界卫生组织的定义,骨质疏松症是指骨矿物质密度 (BMD) 与年轻人的值相比小于两个半标准差 (T ≤ -2.5),是一种病理状况,其特征是骨密度增加全球发病率。
维生素 D 在维持骨骼系统健康方面具有公认的作用,这要归功于它对矿物质和骨骼代谢的直接和间接影响,这是通过与其在血浆中表达的特定受体(维生素 D 受体,VDR)的相互作用介导的某些特定靶器官的细胞膜。事实上,维生素 D 与骨组织细胞中表达的 VDR 相互作用会产生整体合成代谢作用;维生素 D 在肠道水平的作用转化为钙从肠腔向血液的主动转运增加,肠道钙吸收增加,骨钙化过程中这种矿物质的整体可用性增加;
然而,在过去几十年中,大量研究清楚地表明,VDR 不仅在维生素 D 作用的经典器官(骨、肠、甲状旁腺)的细胞中表达,而且在许多其他组织中也有表达 [63 ]。因此,除了维生素 D 对矿物质和骨代谢的典型作用外,还表明维生素 D 可能对许多其他一般病理状况具有有益作用。事实上,观察性研究广泛报道,维生素 D 水平低与患心血管疾病、癌症、糖尿病、感染、自身免疫和免疫相关疾病、心血管疾病 (CVD) 甚至心血管疾病的风险增加有关任何原因导致的死亡率增加 。此外,大量研究还报道,维生素 D 血清水平通常低于医学研究所定义的足以避免任何相关病理效应的浓度阈值。
由于所有这些原因,维生素 D,无论是否与钙补充有关,都越来越频繁地开给骨密度低的患者,尤其是骨质疏松症患者,并且越来越多的食物和/或饮料富含维生素 D。然而,有必要指出,尽管人们普遍热衷于建议更广泛地使用维生素 D ,但受这些假定的积极多效性影响的推动,完全缺乏支持这些假设优势的证据 。
更重要的是,鉴于迄今为止可用数据的非常矛盾的结果,维生素 D 和钙补充剂对骨骼健康的实际作用,特别是对可能降低骨折风险的作用长期以来一直存在争议 [79 ] , 80 , 81 , 82 , 83 ]。最近,一项大规模多中心研究质疑补充维生素 D 和/或钙盐在预防骨质疏松症患者骨折风险方面的作用。
无论如何,就 UL 风险而言,大多数临床试验并未显示维生素 D 和钙补充剂与患尿路结石疾病的风险之间存在任何显着关联,至少在普通人群中是如此。(这方面将在下面讨论)。
4. UL 患者补充维生素 D 和/或钙的建议
如前所述,低骨量的发现在 SF 患者中尤为常见,尤其是那些表现为HC的患者[ 40、43、50、55、56、57、59 ]。此外,据报道,有 UL 病史的受试者特别容易发生骨折,在长达 30 年的观察期内报告的骨折发生率几乎是没有 UL 受试者观察到的四倍,与年龄相匹配和性别 [ 58]. 此外,据报道,维生素 D 缺乏或不足在 UL 患者中比在普通人群中更常见,近 90% 至 30% 的 SF 患者的 25-OH-vit D3 水平低于 30 和 12 ng/mL。由于 SF 患者也更容易患上 CV 疾病,因此也有人声称服用维生素 D,由于其所谓的 CVD 保护作用,可以起到预防此类并发症的作用。此外,似乎这还不够,一些实验数据表明炎症、氧化应激和血管生成参与了 UL 过程的发展。因此,维生素 D 的假定抗炎、抗氧化和抗血管生成活性甚至可以帮助预防结石过程本身。基于所有这些考虑,我们可以争辩说,SF 受试者很容易被认为是维生素 D 处方的理想目标。
另一方面,我们不能忘记,如前所述,SF 受试者的特征通常是尿液中钙和草酸盐排泄增加,维生素 D 和/或钙补充剂也会增加尿钙。
然而,大多数(尽管不是全部)少数随机对照试验报告暴露于维生素 D 和钙补充剂的受试者发生 UL 事件,给出了明显令人放心的信息(表格1):他们声称与未治疗的患者相比,接受治疗的患者的 UL 发生率没有实质性差异。
然而,值得对这些研究的一些特定局限性进行实质性考虑 。
首先,这些研究大多是在老年人中进行的,主要是女性受试者,这些并不是典型的 UL 患者人群的特征,这些患者通常是年轻人或中年人,男性更常见。其次,所有报告 UL 发生率无差异的研究的持续时间均低于 3 年,因此不能排除在较长观察期的情况下,可以观察到治疗组和未治疗组之间的一些差异。最后,不清楚有多少患者有既往 UL 事件史;因此,当向已经发生一次或多次 UL 事件的患者开出此类补充剂时,就 UL 发生的风险可能是什么得出任何结论是相当武断的,这代表了这种临床情况下的真正医学问题。
5. UL 患者补充维生素 D 和/或钙的风险
根据之前报告的数据,当向有肾结石病史的患者开具维生素 D 和/或钙补充剂时,担心 UL 风险增加的理由非常充分,尤其是对于那些患有任何类型 HC 的患者.事实上,补钙,尤其是在饭后补钙,可以增加肠道吸收的钙量,留下更多的草酸盐供吸收。这导致尿钙排泄增加和尿草酸盐可能增加(图 2). 另一方面,补充维生素 D 可以增加钙、草酸盐和磷酸盐的肠道吸收,从而增加所有这三种成分的尿液排泄,因此可能增加草酸钙和钙的相对饱和度。磷酸盐(图 3).许多实验和观察数据都证实了这一点。我们将仅限于引用一些最近的发现,这些发现支持与维生素 D 和/或钙补充剂相关的潜在增加的结石风险的概念。在小鼠中针对 ABCC6 基因进行了一项优雅的实验研究,该基因编码了一种转运蛋白,可增加焦磷酸盐的细胞外可用性,焦磷酸盐是最有效的异位钙化抑制剂之一。作者得出结论,补充维生素 D 和钙会加速兰德尔氏斑的形成,这是草酸钙结石过程的起点。在对 25(OH)D 水平低于 20 ng/mL 的 33 名 SF 患者进行的一项实验研究中,补充胆钙化醇可有效使 25(OH)VitD 血清水平正常化(从 11.8 ± 5.5 到 40.2 ± 12.2 ng/mL),导致尿液中草酸钙和透钙磷石的过饱和度显着增加。最近的一项审查和荟萃分析包括涉及 23,228 名参与者的 32 项观察性研究,报告说,与对照组和没有 HC 的 SF 受试者相比,患有 HC 的 SF 受试者的循环 1,25(OH)VitD3 和 25(OH)VitD3 水平增加。更重要的是,一项大型随机对照试验旨在探索维生素 D 和钙补充剂的长期(随访 7 年)效果,并在 36,282 名绝经后妇女中进行。结果显示,与接受安慰剂治疗的患者相比,接受维生素 D 和钙补充剂的患者发生 UL 的次数显着增加(表格1)。
另一点值得特别注意的是,由于参与维生素 D 代谢或活性的基因的某些遗传变异,一些受试者对维生素 D 的毒性作用易感。
在他们的开创性研究中,Schlingmann 及其同事在六名患有自发性高钙血症和还在一组新生儿中发现,在这些新生儿中,维生素 D 给药后出现了严重的高钙血症 [ 98 ]。从那时起,许多研究报告了形成尿路结石的风险增加与 CYP24A1 基因、VDR 基因多态性或某些特定溶质转运蛋白(SLC34A1、SLC34A3)的其他遗传变异之间的强烈关联,这表明一些个体可能比其他人更容易遭受服用维生素 D 的促结石作用 。这些新发现促使一些同事建议,在为 UL 患者开出饮食和/或补充剂处方时,应用营养遗传学和营养基因组学方法可能是合适的。基于这种病理生理学背景,许多作者表达了他们对给 SF 患者开此类补充剂的担忧,特别是那些同时患有高钙尿症的患者。
六、结语
试图就肾结石形成人群中维生素 D 和/或钙补充剂的安全性得出一些明确的结论,我们应该首先假设没有明确的证据表明维生素 D 和钙补充剂会导致或没有潜在的负面影响关于在普通人群中促进 UL 发生的风险。在处理具有 UL 病史的患者时,缺乏关于这样一个关键问题的一致和可靠的信息,因为这些患者只是偶尔被包括在大多数进行的最大的对照试验中,尽管他们经常接受这样的治疗处方,因为他们很容易患骨质疏松症。还应该考虑的是,即使最近的研究对维生素 D 和钙补充剂对骨骼健康的功效提出了一些质疑,也不容易接受不纠正严重的维生素 D 缺乏症,即使是在有 UL 病史和患有当代骨折的高风险。
在这些情况下,任何医生都很难平衡一方面是骨骼的潜在风险,另一方面是肾结石形成的风险。因此,Sundeep Khosla 十多年前就已经提出的问题 [ 110 ] 关于这些患者的实际方法应该是什么仍然没有答案。没有任何想就此主题提供任何指导的假设,我们将限制自己与读者分享我们对这个问题的务实方法。首先,我们考虑开具维生素 D 和钙补充剂处方的适应症强度,在我们看来,这表现为 BMD 严重降低(T 值 < -2.5)和/或维生素 D 水平低于 15 ng/ mL 和/或慢性和严重的吸收不良疾病。如果有治疗指征,我们应该在 Rule 和合作者几年前发布的列线图的帮助下,评估每个受试者发生 UL 的风险,或者如果患者已经是 SF,则评估他/她的复发风险。图 4说明了我们的 UL 风险分层模型,其中有强烈的迹象表明要开维生素 D 和/或钙补充剂,以及我们建议采取的行动。
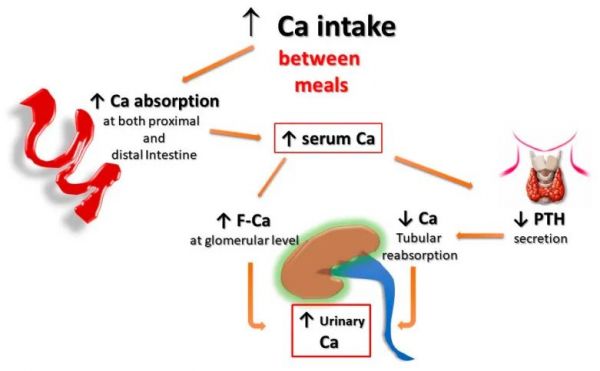
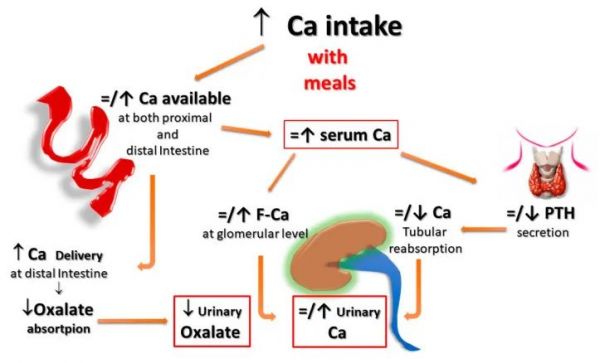
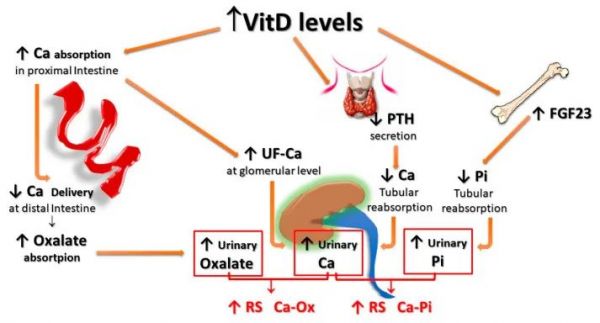
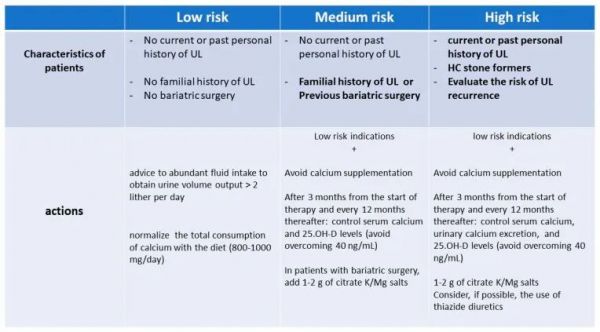
图 4 UL 风险的定义和建议在有强烈迹象表明需要服用维生素 D 和/或钙补充剂的受试者中采取的行动。鉴于该实用算法的可疑性,我们还建议随着时间的推移在每个个案中重复此评估,权衡收益风险比。即,应将治疗对骨骼健康参数的有效性与安全参数进行比较,特别是关于结石风险、评估尿钙排泄的变化和/或高钙血症的出现或新发或结石事件的复发.通常,在大多数关于有争议主题的评论结束时,作者建议并希望开始专门的试验。然而,由于我们很清楚目前开展此类研究存在的困难,我们希望更系统和共享地收集 UL 患者的临床随访数据,提交补充维生素 D 和/或钙的治疗,可以付诸行动,可能共享一些预防协议。这可以提高医生在该临床实践领域的知识,并有望提高对此类患者的护理效果。
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
维生素D和钙补充剂与尿石症:有争议和多方面的关系
如何补充钙与维生素D
孕妇维生素d每天补充多少钙
关于维生素补充剂,你了解多少?
孕期补充维生素D的方法
大剂量补充维生素D对骨密度和骨强度的影响
如何科学补充维生素D?了解这2点,才有补钙效果
维生素D怎么补?补充维生素D,你不可不知的7个问题!
没想到,补充维生素D也有这么多学问
宝宝补钙关键是补充维生素D 盘点常见维生素D保健品
网址: 维生素 D 和钙补充剂与尿石症:一个有争议的多方面关系 https://m.trfsz.com/newsview243226.html