采用泡沫分离技术从茶多酚废液中提取茶氨酸的工艺的制作方法
本发明涉及一种提取茶氨酸工艺,特别涉及一种采用泡沫分离技术从茶多酚废液中提取茶氨酸的工艺。
背景技术:
茶氨酸(l.theanine)是一种手性非蛋白质氨基酸,是1950年日本学者酒户弥二郎在研究玉露茶鲜爽滋味成分的过程中发现的,占茶叶干重的l%-2%,占茶叶中游离氨基酸总量酌40%-70%,被称为“天然镇静剂”。茶氨酸在医学上用于抗肿瘤辅助药物,抗糖尿病,调节情绪和降血压,减轻酒精对肝脏的伤害。茶氨酸在食品行业用作功能性、风味食品添加剂、茶饮料的品质改良剂。茶氨酸还有减肥、抗疲劳、保护心脑血管以及作为净水剂净化饮用水和化妆品中的保湿剂等功能。茶氨酸是21世纪的健康食品。目前茶氨酸的主要制备途径有:提取分离法、化学合成法、细胞组织培养法及微生物发酵法;提取分离纯化的方法主要有:试剂沉淀法、离子交换树脂法、大孔吸附树脂法、膜分离法、双水相萃取、高效液相色谱制备法、结晶法、泡沫分离技术。
泡沫分离技术又被称为吸附泡沫分离技术,是以气泡为载体来分离、浓缩表面活性物质的一种技术。泡沫分离技术最早应用于矿物浮选以及工业废水中有用添加剂的回收。70年代才开始将泡沫分离技术引入生物分离领域,如蛋白质及酶的分离纯化。在分离过程中不需要添加其他溶剂,只需通入空气或是其他惰性气体即可;适合处理稀溶液,而且能够得到较高的富集比。目前利用泡沫分离技术提取分离茶氨酸的报道较为少见。利用泡沫分离技术从茶多酚废液中提取分离茶氨酸的研究工艺尚未出现报道情况。从茶多酚废液中进一步提取分离茶氨酸可以实现资源再利用。
研究表明目前,泡沫分离技术已在金属制造业和渔业中实现了工业化生产。在食品工业及生化研究中,泡沫分离技术已被用于蛋白质、多糖及其他生物活性物质等的分离提取,但多处于实验室研究阶段,泡沫分离氨基酸报道较少。
技术实现要素:
本发明所要解决的技术问题在于提供一种采用泡沫分离技术从茶多酚废液中提取茶氨酸的工艺,以解决泡沫分离和重结晶等技术处理茶叶粗提液获得茶氨酸的工艺条件中的实际技术问题。
为了实现上述技术目的,本发明的设计方案如下:
一种采用泡沫分离技术从茶多酚废液中提取茶氨酸的工艺,包括以下步骤:
(1)对茶多酚废渣浸提,制得含滤渣浸提液;
(2)将步骤(1)制得的含滤渣浸提液进行抽滤,得到浸提液;
(3)向步骤(2)制得的浸提液中加入乙酸乙酯进行萃取,分离后,水相液体备用;
(4)向步骤(3)制得的水相液体中添加十二烷基硫酸钠进行起泡,接着进行震荡气泡离子交换,将茶氨酸置换到泡沫中,收集泡沫;
(5)将步骤(4)收集到的泡沫采用无水乙醇消泡并冷冻结晶,待去除上清液后,获得沉降结晶;
(6)将步骤(5)制得的结晶离心真空冷冻干燥或鼓风干燥,收集干燥后的晶体重结晶,接着干燥,制得茶氨酸。
进一步地,步骤(1)中对茶多酚废渣浸提的条件:浸提温度为恒温水浴80-100℃,料液比为1:10-30,浸提时间为30-60min。
进一步地,步骤(4)中所述十二烷基硫酸钠的添加量为1-2g。
进一步地,步骤(4)中震荡的条件:在恒温水浴振荡器中震荡气泡,水浴温度为25-30℃,震荡频率180r/min。
进一步地,步骤(4)中气泡离子交换时间为20-40min。
进一步地,所述气泡离子交换时间为30-35min。
进一步地,步骤(5)中无水乙醇的质量浓度为95%,无水乙醇的加入量为泡沫溶液体积的2-4倍。
进一步地,步骤(5)中冷冻结晶的条件:在0-5℃下冷冻24h结晶。
进一步地,步骤(6)中离心的速率为8000rpm,冷冻干燥是在60℃下进行的,鼓风干燥是在95℃下进行的。
进一步地,步骤(6)中收集干燥后的晶体重结晶的方法如下:取干燥后的晶体用蒸馏水配成20%的溶液,再加入3-4倍体积的无水乙醇,在常温下振荡混匀后,静置1-2h,用离心率为8000rpm离心机离心去除产生的沉淀,离心清液60℃减压浓缩为80%的溶液,冷却后加4倍体积的无水乙醇,0℃下冷藏24h,产生结晶状物质,在4℃和离心速率为8000rpm下离心得类白色固体,将所得固体用热水溶解,同上述方法重结晶3次。
通过本技术方案,可以实现以下效果:
(1)本发明利用添加十二烷基硫酸钠在液体中震荡起泡,吸附液体中的茶氨酸等物质,使之实现固液分离;通过进一步的研究,从众多表面活性物中筛选出了合适本发明工艺的表面活性物——十二烷基硫酸钠,已达到了较好的分离效果,解决了泡沫分离和重结晶等技术处理茶叶粗提液获得茶氨酸的工艺条件中的关键问题。
(2)本发明从废液废渣中提取出茶氨酸,为后面研究茶氨酸提供一种新的技术方法参考;同时利用泡沫分离技术对茶多酚废液中的茶氨酸物质进一步回收,提高了经济效益。
【附图说明】
图1是茶氨酸标准曲线图;
图2是不同浓度十二烷基硫酸钠对茶氨酸提取率的影响图;
图3是不同起泡时间对茶氨酸提取的影响图;
图4是不同料液比对茶氨酸提取的影响图;
图5是不同的浸提温度对茶氨酸提取的影响图;
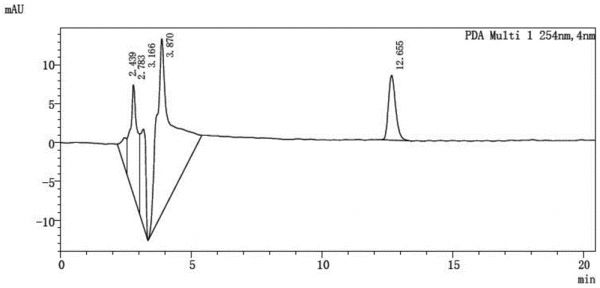
图6是茶氨酸标准样品高效液相色谱图;
图7是样品中茶氨酸高效液相色谱图。
【具体实施方式】
1材料与方法
1.1试剂与材料
茶多酚废渣:茶叶贺州昭平绿茶,贺州学院食品与生物工程学院有机化学实验室。
标准样品:纯度99%以上的茶氨酸,采购于北京索莱宝科技有限公司。
添加剂:十二烷基硫酸钠。
所用试剂如:无水乙醇;乙酸乙酯,乙酸,甲醇,茚三酮,丙酮;诺无特别说明均为分析纯ar。
1.2主要设备
高效液相色谱仪(株式会社岛津制作所,日本);dhg-9240a型电热恒温鼓风干燥箱(上海跃进医疗器械有限公司);ar224cn型电子分析天平(上海舜宇科学仪器有限公司);jj500型电子天平(江苏常熟徐市);hh-s4型恒温水浴锅(上海博讯实业有限公司医疗设备厂);shz-d(ⅲ)循环水式真空泵(巩义市予华仪器有限公司);fz102型粉碎机(河北省黄马华市新兴电器厂);zwy110x30恒温水浴震荡器;fz102型粉碎机(河北省黄马华市新兴电器厂)h1850r台式高速冷冻离心机(湖南湘仪实验室仪器开发有限公司)。
1.3茶氨酸提取率测定方法
1.3.1茶氨酸的提取工艺流程
茶多酚废渣→浸提→抽滤→浸提液→乙酸乙酯萃取→水相→添加表面活性物→起泡→收集泡沫→消泡→无水乙醇沉淀(0-5℃24h)结晶沉降→去除上清液→离心真空冷冻干燥或鼓风干燥→茶氨酸→分析检测。
所述茶氨酸的提取工艺,包括以下步骤:
(1)对茶多酚废渣浸提,浸提的条件:浸提温度为恒温水浴80-100℃,料液比为1:10-30,浸提时间为30-60min,制得含滤渣浸提液;
(2)将步骤(1)制得的含滤渣浸提液进行抽滤,得到浸提液;
(3)向步骤(2)制得的浸提液中加入乙酸乙酯进行萃取,分离后,水相液体备用;
(4)向步骤(3)制得的水相液体中添加十二烷基硫酸钠进行起泡,添加量为1-2g,接着进行震荡气泡离子交换,震荡的条件:在恒温水浴振荡器中震荡气泡,水浴温度为25-30℃,震荡频率180r/min,气泡离子交换时间为20-40min,将茶氨酸置换到泡沫中,收集泡沫;
(5)将步骤(4)收集到的泡沫采用质量浓度为95%的无水乙醇消泡并冷冻结晶,无水乙醇的加入量为泡沫溶液体积的2-4倍,冷冻结晶的条件:在0-5℃下冷冻24h结晶,待去除上清液后,获得沉降结晶;
(6)将步骤(5)制得的结晶离心真空冷冻干燥或鼓风干燥,离心的速率为8000rpm,冷冻干燥是在60℃下进行的,鼓风干燥是在95℃下进行的,取干燥后的晶体用蒸馏水配成20%的溶液,再加入3-4倍体积的无水乙醇,在常温下振荡混匀后,静置1-2h,用离心率为8000rpm离心机离心去除产生的沉淀,离心清液60℃减压浓缩为80%的溶液,冷却后加4倍体积的无水乙醇,0℃下冷藏24h,产生结晶状物质,在4℃和离心速率为8000rpm下离心得类白色固体,将所得固体用热水溶解,同上述方法重结晶3次,接着干燥,制得茶氨酸。
1.3.2茶氨酸标准曲线的绘制
分别准确吸取茶氨酸标准储备液(1mg/ml)0.0、0.1、0.2、0.5、1.0、1.5ml,用水定容至10ml,此标准系列的浓度为0.0、0.01、0.02、0.05、0.10、0.15、0.20mg/ml的茶氨酸标准系列溶液,进样分析,用峰面积对浓度进行线性回归,表明在给定的浓度范围内茶氨酸检测呈线性,如图1所示,回归方程为y=32321x+589825,(y为峰面积,x为浓度,μg/ml):线性相关系数r2=0.9995。
1.3.3茶氨酸总量的测定
准确称量10.0000g茶多酚废渣,固定液料比为1:20ml/g,水浴加热时间45min,水浴浸提温度为80℃,将浸提液冷却后抽滤,将抽滤后的提取液转移至分液漏斗中,加入相同体积的乙酸乙酯,充分混匀静置直到分层完毕,取下相液体,将相提取液浓缩到100ml;添加十二烷基硫酸钠1.5g,起泡30min,收集泡沫,消泡,加入2-3体积乙醇重结晶,计算重量,加入离子水溶解定容到100ml,第一次待测液取2.0ml加入10ml容量瓶中,利用高相液相色谱仪进行测定,第二次、第三次待测液取5.0ml进行测定,每次平行测定三次,取其平均值,计算每次测得的茶氨酸含量,把几次测得的茶氨酸含量总和加起来作为茶多酚废渣中茶氨酸的总量。滤液中茶氨酸含量的计算公式为:
式中:
m—待测液中茶氨酸含量(mg/g);
c—待测液溶液浓度(μg/ml);
v—提取液体积(ml);
v1—定容体积(ml);
w—样品的干重(g)。
1.3.4茶氨酸提取率的测定
准确称量10.0000g茶多酚废渣,固定液料比为1:20ml/g,水浴加热时间45min,水浴浸提温度为80℃,得到茶浓缩液。将浸提液冷却后抽滤,将抽滤后的提取液转移至分液漏斗中,加入相同体积的乙酸乙酯,充分混匀静置直到分层完毕,取水相脱除有机溶剂后制得茶浸提液,备用。将获得的水相置于250ml锥形瓶中,添加入十二烷基硫酸钠1.5g,搅拌均匀,再将其混匀转至恒温水浴振荡器(180r/min,25℃)中进行震荡起泡,30min后收集泡沫,进行消泡处理,再用95%乙醇沉淀(0-5℃冷藏24h重结晶),去除上清液,8000rpm离心,收集晶体,将所得晶体在60℃下进行真空干燥或者95℃鼓风干燥,得到茶氨酸样品,加入水将其溶解并定容至25ml容量瓶中,过膜利用高效液相色谱仪检测其吸收值,计算浓度与产率。
式中:
x—样品中茶氨酸的提取率(%);
m—待测液中茶氨酸含量(mg/g);
m—样品中茶氨酸的总量(mg/g)。
1.4单因素对茶氨酸提取率影响试验方法
以十二烷基硫酸钠添加量、起泡时间、料液比、浸提时间;4个因素为自变量,茶氨酸提取率为考察指标,通过固定其他3个因素,改变某一因素的取值,平行重复测定三次,确定相关因素的影响,并为后续正交试验设计提供各个因素的取值范围,本研究水浴温度为80℃,震荡气泡条件为(180r/min,25℃)。
1.4.1单因素试验考察不同十二烷基硫酸钠添加量对茶氨酸提取率的影响
取十二烷基硫酸钠添加量为1g、1.25g、1.5g、1.75g、2g;固定起泡时间30min,料液比1:20,浸提时间45min;进行提取实验,考察不同浓度十二烷基硫酸钠对茶氨酸提取率的影响,结果如图2所示。
由图2可知,茶氨酸提取率随着十二烷基硫酸钠的增大而增大,当到达一定比例后,茶氨酸提取率曲线呈现缓慢下降。这是因为十二烷基硫酸钠的上升在一定程度上提高了传质推动力,起泡置换效果更佳;而十二烷基硫酸钠超过1.75g后,不仅会有一部分杂质也被提取出来,也造成茶氨酸的提取率下降,所以曲线呈下降现象。故选择十二烷基硫酸钠1.75g最适宜。
1.4.2单因素试验考察不同起泡时间对茶氨酸提取率的影响
取起泡时间为20min、25min、30min、35min、40min;固定十二烷基硫酸钠添加量为1.5g,料液比1:20,浸提时间45min;进行提取实验,考察不同起泡时间对茶氨酸提取的影响,结果如图3所示。
由图3可知,茶氨酸提取率随着起泡时间的增大而增大,当到达一定值后,茶氨酸提取率曲线呈现快速下降。这是因为起泡时间的上升在一定程度上提高了对茶氨酸分子的置换能力,而十二烷基硫酸钠超过35min后,不仅会有一部分杂质也被提取出来,而且会影响茶氨酸在泡沫的存在,被其他物质置换出来,造成茶氨酸的提取率下降,所以曲线呈下降现象。故选择起泡时间为35min最适宜。1.4.3单因素试验考察不同料液比对茶氨酸提取的影响
取料液比为1:10、1:15、1:20、1:25、1:30;固定十二烷基硫酸钠添加量为1.5g,浸提时间45min,起泡时间30min;进行提取实验,考察不同料液比对茶氨酸提取的影响,结果如图4所示。
由图4可知,茶氨酸提取率随着料液比的增大而增大,当到达一定值后,茶氨酸提取率曲线呈现缓慢下降。这是因为料液比的上升在一定程度上提高了传质推动力,而料液比超过1:20之后,不仅会有一部分杂质也被提取出来,溶液中物质提取增加,会造成部分被提取出来的茶氨酸损耗,造成茶氨酸的提取率下降,所以曲线呈下降现象。故选择料液比1:20最适宜。
1.4.4单因素试验考察不同浸提时间对茶氨酸提取的影响
取起浸提时间为30min、37.5min、45min、52.5min、60min;固定十二烷基硫酸钠添加量1.5g,起泡时间30min,料液比1:20;进行提取实验,考察不同的浸提温度对茶氨酸提取的影响,结果如图5所示。
由图5可知,在52.5min以下茶氨酸的提取率随着温度的升高而增大,说明在一定的范围内升高温度有利于茶氨酸的溶出,这是因为温度升高,茶氨酸溶出速率加快,52.5min后曲线趋于下降。这是因为提取时间过久,氨基酸容易产生变性,目标产物有损耗,因此选择浸提温度52.5℃最适宜。
1.5茶氨酸提取工艺条件优化试验方法
茶氨酸提取工艺条件优化试验方法采用正交分析法。
1.5.1正交分析试验设计
从单因素试验中确定对茶氨酸提取率影响最大的主次因素,选定其中3个因素的零水平与波动区,以茶氨酸提取率为考察指标,得出最佳提取工艺条件。1.5.2茶氨酸提取最佳工艺条件验证
通过正交试验分析法优化得到最佳提取工艺条件,结合实际,运用最佳工艺条件进行提取验证试验,平行测定三次。
2试验结果与分析
2.1茶氨酸标准曲线回归方程
按照1.3.2试验方法绘制茶氨酸标准曲线,曲线见图1。
由图1可知,得到茶氨酸标准曲线回归方程和相关系数为:
y=32321x+589825;r2=0.9995
式中:
y—峰面积;
x—标准溶液浓度(mg/ml)。
2.2茶多酚废渣中茶氨酸总量的测定结果
根据1.3.2中的试验操作,利用高效液相色谱仪,计算每次测得待测液中的茶氨酸浓度,得出茶氨酸含量,把三次测得的茶氨酸含量总和加起来取平均值作为样品中单宁的总量。茶氨酸的总量m(mg/g)=(m1+m2+m3)/3;
2.3单因素试验结果
由单因素实验结果可知,十二烷基硫酸钠1.75g,起泡时间35min,料液比1:20,浸提温度52.5min,有最高值,故在此条件较为适宜。
2.4正交试验分析
2.4.1正交试验因素水平
根据单因素试验结果可知,对一定量的茶多酚废渣进行提取实验,采取3个不同的十二烷基硫酸钠添加量(1.5、17.5、2g);三个不同的料液比(1:20、1:25、1:30/ml)和三个不同的浸提时间(37.5、45、52.5min),用三因素三水平正交试验进行茶氨酸提取优化试验,以十二烷基硫酸钠添加量、液料比、浸提时间三个因素作为变量,以茶氨酸的提取率作为考察指标。
表1试验因素与水平
2.4.2试验方案
正交试验方案详见表2
表2正交试验方案
由正交试验分析可知,当提取条件为a1b2c2时,即十二烷基硫酸钠添加量为1.5g,料液比为1:25,浸提时间为45min时,在高效液相色谱仪中会有最大吸收峰值出现,结合线性回归方程可知茶氨酸的提取量和提取率都是最大的,提取率达到67.91%,纯度为73.51%。
3各项检测条件确定
3.1高效液相色谱最佳洗脱条确定
按照1.3.2节方法进行测定实验,最终确定的分离最好流动相条件,离子水:甲醇=1:0.75(v/v),液相甲醇浓度为75%,流速为1ul/min,柱温40℃,峰时间12.5min左右,检测波长254nm。
3.2样品实测情况
由图2显示,茶氨酸标准样品经衍生后测定,标准样品在12:30-13:00min之间有最大吸收峰值,经检测待测样品在12:749min有最大吸收峰值;图3样品中茶氨酸的测定显示高效液相色谱图,茶氨酸衍生物出峰前后无其他氨基酸衍生物干扰,此方法可用作茶氨酸准确定性及定量的测定方法。
利用正交优化试验,无水乙醇重结晶三次以上,进一步纯化可得纯度达到89.42%的茶氨酸样品。
以上所述,仅是本发明的较佳实施例而已,并非对本发明的技术范围作任何限制,故但凡依本发明的权利要求和说明书所做的变化或修饰,皆应属于本发明专利涵盖的范围之内。
相关知识
豆制品加工废水处理工艺
茶叶的保健作用
中医与茶疗:茶疗“治未病”在养生保健中的应用价值
白茶泡水喝的功效
哪些茶可以养生保健 保健茶冲泡方法
春茶飘香,你真的会健康饮茶吗?
有机茶种植技术要点(建议收藏)
茶中之王大红袍的品鉴方法
一种有机茶树的生态健康的种植方法
效果好的减肥茶排行榜及配方:无副作用减肥茶推荐
网址: 采用泡沫分离技术从茶多酚废液中提取茶氨酸的工艺的制作方法 https://m.trfsz.com/newsview372775.html