AHA科学声明:非心脏手术后心肌损伤患者的诊断和治疗策略



1:在基线肌钙蛋白值异常的患者中,若在非心脏手术后,cTnI或cTnT升高20%,高敏cTnT绝对值较术前值升高≥14ng/L,或高敏cTnT较先前的浓度增加≥5ng/L,伴高敏cTnT峰值>20ng/L,可判定为急性心肌损伤。预后的重要阈值应被考虑,而不是特定cTn分析的第99百分位数值的URL:非高敏第四代肌钙蛋白T≥30ng/L(Roche 第四代Elecsys TnT分析),高敏肌钙蛋白T值从20至<65ng/L,绝对值变化≥5ng/L,或高敏肌钙蛋白T浓度≥65ng/L(Roche Elecsys 高敏肌钙蛋白T分析)
二、MINS的定义 MINS的定义是,在缺乏明显的非缺血性证据时(如肺栓塞),由于一项假定的缺血机制(如供需不匹配或动脉粥样硬化),术后至少1项cTn浓度超过cTn分析的第99百分位数值参考范围的上限。cTn数值升高须在术后首个30d内识别,但数值升高几乎总是出现于术后首个2d内。临床症状和心电图变化并非是诊断MINS的必要条件,MINS包括心肌梗死和缺血性心肌损伤。 一系列的cTn浓度对识别急慢性心肌损伤是有必要的,术前cTn浓度是术后测量比较的依据。对临床心血管事件高风险患者,如年龄≥65岁或年龄≥45岁但已证实患有冠状动脉或外周动脉粥样硬化心血管疾病,若测量结果将改变临床治疗策略,推荐纳入术前cTn基线测量,且在术后48h至72h重复测量1次。当术后cTn浓度升高,但无近期(术前或术后)cTn测量值时,应纳入第二次cTn测量,以确定是否存在通过升高或降低模型表明急性心肌损伤的存在。在术前或术后最初测定的cTn值超过第99百分位数值的患者中,若随后cTn浓度有>20%的升高或降低,则心肌损伤被判定为急性的。该>20%阈值最初是在心肌梗死的普遍定义中提出的,用来在非手术队列中,识别cTn发生的变化大于预期的分析变异率,以评估非手术队列中的再梗阻。尽管同其他心肌梗死亚型的指南一致,但>20%阈值是基于专家共识,尚未在手术背景下被证实。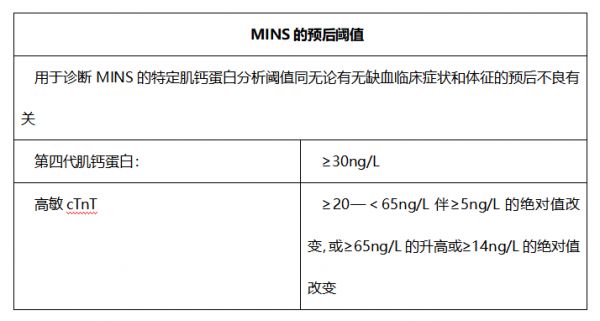
非心脏手术后发生心肌损伤很常见。在一项纳入了21842例年龄≥45岁且住院期间接受非心脏手术患者的国际性的多中心研究(VISION研究,在非心脏手术患者队列评估的血管事件)显示,18%的患者会进展为MINS。当使用传统第四代TnT分析时,MINS发生率为8%。在一项纳入2018例年龄≥65岁或年龄≥45岁且有血管疾病病史患者的单中心研究中,16%的患者会进展为MINS。总而言之,一项纳入530867例手术预后结果的169篇已发布的近期系统性回顾中,MINS综合发生率为18%。在一项使用系统性cTn测量的大型前瞻性系列分析中,20%的手术人群会并发MINS。
有几项因素影响已报道的MINS发生率。第一,MINS的定义随研究不同而发生改变。一些评估MINS的研究会排除假定的由非缺血性原因导致术后心肌损伤的患者,然而其他研究包括所有患心肌损伤的患者。第二,MINS的发生率也取决于是否进行系统性术后cTn监测,84%~93%的MINS患者并不表现出可识别的缺血症状。进行或不进行系统性cTn监测的研究,所报道的MINS的发生率分别为20%和10%。监测时机也会影响MINS的发生频率。来自VISION的数据显示,78%的MINS发生于手术日或术后首日,94%的MINS发生于术后第二天,仅有0.6%的MINS发生于术后第三天。第三,所使用的cTn分析方法也会影响MINS的发生率。相较于传统的分析方法,使用高敏cTn分析方法检测出的MINS发生率更高。在一项常规使用术后cTn检测的系统性回顾研究中,使用hsTnT分析时MINS的发生率为25%;使用传统的第三或第四代cTnI分析,MINS发生率为20%;使用传统的TnT分析,MINS的发生率为17%。最后,手术人群也会影响MINS的发生率,其发生率可能会随年龄、性别、肾功能和接受手术的紧急情况而发生改变。
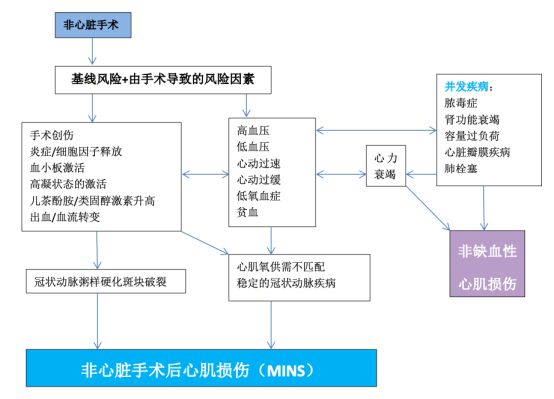
四、MINS的特定病因 通过MINS的定义可以得知,导致MINS发生的原因有缺血原因(例如,血液供需不匹配或冠状动脉粥样硬化)。许多因素可导致非心脏手术后cTn值升高。麻醉和手术创伤可导致儿茶酚胺、皮质醇和炎症细胞因子的增加。围手术期血流动力学紊乱可引起心肌氧供需不平衡发生缺血从而导致心肌损伤。心动过速会降低心脏舒张期的持续时间,增加心室壁压力和氧需。高血压会增加左心室后负荷和心肌氧需。冠状动脉剪切应力的增加会破坏原先存在的冠状动脉粥样硬化斑块稳定性,引起斑块破裂(侵蚀或破碎)。在冠状动脉稳固狭窄的情况下,由低血压和心动过缓引起的冠状动脉灌注压的降低也会导致心肌氧供需的严重不匹配。血小板激活增加和高凝状态有助于血栓形成的环境。血管炎症、内皮功能紊乱和冠状微血管疾病也可能会引起心肌损伤。综合来看,这些巨大的病理生理改变促进围手术期心血管风险的增加。在大部分病例中,MINS与冠状动脉疾病(CAD)有关。MINS可能是由斑块破裂引起,无论是否有血栓形成,导致Ⅰ型心肌梗死或心肌损伤;或在无不稳定斑块存在的情况下,冠状动脉灌注和心肌氧需不匹配导致Ⅱ型心肌梗死。心肌损伤可能出现于稳定型梗阻性CAD或非梗阻性斑块中,伴或不伴有内皮功能紊乱和冠状动脉微血管疾病。一项患者接受非心脏手术前进行冠脉CT造影的研究发现,术后发生心肌梗死的患者中,72%的患者患有梗阻型冠心病,而这些患者中仅有4%无CAD。在接受非心脏手术后,发生围手术期心肌梗死或MINS而进行冠脉造影的患者中,77%~94%的患者存在梗阻型CAD。其他血管造影系列的研究也表明,MINS通常与原先存在的梗阻型CAD或不稳定斑块有关。在尸检结果中,46%的接受非心脏手术后发生致命性心肌梗死的患者,有冠状动脉斑块破裂的证据。
其他几项普遍存在于患有MINS的手术队列中的心血管风险因素,可能构成了围手术期cTn值升高的发病机制。患有阻塞性睡眠呼吸骤停的患者易发生心血管事件,可能是由内皮功能紊乱、高血压、血管效应激素的浓度升高以及偶发性低氧血症介导的。在1218例阻塞性睡眠呼吸暂停风险的患者中,在接受重大非心脏手术后随访30d内,严重阻塞性睡眠呼吸暂停与MINS有关。其他与MINS有关的风险因素包括糖尿病、充血性心力衰竭和已经存在的冠心病。贫血在心肌氧供需不匹配的情况中也起到重要作用。肾功能衰竭是MINS的一项独立风险因素,使用一项传统的非hsTnT分析评估,发现围手术期预估的肾小球滤过率和MINS发生率存在阶梯式关联。相较于预估的肾小球滤过率为≥60ml•min-1•1.73m-2的患者,预估肾小球滤过率为45~59、30~44和<30ml•min-1•1.73m-2的患者,其MINS的风险因素分别增加1.7(95%CI 1.4~2.0)、2.4(95%CI 2.0~2.9)和7.9(95%CI 6.7~9.3)。
部分情况可能通过非缺血性心肌损伤混淆MINS的诊断。围手术期脓毒症能直接介导心肌损伤和心肌病。总而言之,在患有脓毒症的患者中,不应贸然下MINS的诊断。此外,右心室心肌损伤可能发生于后负荷突然升高,例如患有急性肺栓塞。心肌损伤也在患有急性失代偿性心力衰竭患者中广泛存在。
在术前访视时,麻醉科医师进行主观评估时,为预测MINS会评估患者功能状态等。类似的,通过标准化运动测试的最大化运动能力并不与术后MINS风险有关。然而,自我报告的标准化杜克活动状态指数问卷同MINS的发生有关。尽管有必要进行更进一步的研究证实,但杜克活动状态指数≤34似乎可识别出处于更高风险MINS的手术患者。
动脉粥样硬化性心血管疾病,包括CAD、脑血管疾病或外周动脉疾病以及相关的风险因素(如,高血压、糖尿病)是MINS很强的预测因子。其他几项心血管(心力衰竭、房颤)和非心血管(未经治疗的严重阻塞性睡眠呼吸暂停、术前肾功能受损)并发症也是MINS的独立预测因子。
考虑到个体心血管并发症的预后重要性,包含这些相似并发症的综合预测指标也能预测MINS。例如,修订版的心脏风险指数,包括CAD、心力衰竭、脑血管疾病、糖尿病和肾功能受损,都与MINS的发生独立相关。值得注意的是,基于鼾声、劳累和可观察到的呼吸暂停、高血压、体重指数、年龄、颈围、STOP-BANG分数和男性性别风险指数的高风险分类,最初是为筛查未诊断的阻塞性睡眠呼吸暂停,且包含一些MINS的个体预测指标(如高龄、男性、高血压),在一项大型前瞻性队列研究中,该分类也与MINS的发生独立相关。
除在术前访视时能容易识别的临床特点外,术前实验室检查可以提供MINS风险评估信息。预测MINS的最有力的生物标志物是钠尿肽——BNP(脑钠肽)或NT-proBNP(N-末端-proBNP)。在一项纳入10402例接受非心脏手术且进行术前NT-proBNP测量的前瞻性队列研究中,有378例发生MINS。多变量分析显示,相较于术前NT-proBNP水平<100ng/L(参考组,MINS发生率为5%),NT-proBNP水平较高的患者,其MINS发生风险较高:NT-proBNP为100~200ng/L时,MINS发生率为12%;NT-proBNP200~<1500ng/L时,MINS发生率为20%;NT-proBNP≥1500ng/L时,MINS发生率为36%。此外,一项纳入619例在术前实施BNP检测的手术患者的系统性回顾研究发现,BNP<92ng/L同较低的围手术期风险有关, BNP值更高的患者围手术期死亡和非致命性心肌梗死的风险会增加。
在个别大型队列研究中,用于预测MINS的其他几项实验室测试,包括血糖升高、网状血小板浓度升高(血小板转变的标志)以及中性粒细胞/淋巴细胞的比率>4(全身炎症的标志)。在接受血管手术的患者中,通过负荷心肌灌注影像识别的可逆性缺陷也同MINS发生有关。此外,在术前接受运动试验的患者中,运动后第1min内心率恢复受损(降低≤12bpm),(副交感神经功能紊乱的标志)也与MINS发生风险升高有关。
除患者特定的风险因素外,计划手术的紧急性和类型,对MINS发生风险而言也是重要的决定因素。接受紧急手术或急诊手术的患者,发生MINS的风险会高2~3倍。几项手术类型也同MINS发生风险增加有关,包括血管手术(尤其是开放性主动脉或腹股沟下手术)和普外科腹部手术。在VISION研究中,心肌损伤发生率最高的为血管手术(19%)、骨科手术(12%)、胸科手术(9%)和普外科手术(9%)。



尽管有三项大型旨在评估可降低心血管风险的4种围手术期干预措施(β受体阻滞剂、α2受体激动剂、阿司匹林和笑气)的随机试验,但目前尚无已知的可用来预防围手术期心肌梗死的安全有效方法。这些试验所采用的标准是类似的,都包括年龄≥45岁伴已知或疑似心血管疾病的患者且已被安排住院期间接受非心脏手术。在每一项试验中,由《第3版心肌梗死通用定义》所定义的心肌梗死是主要心血管综合征30d终点的主要组成部分。心肌损伤是一较新的概念,到目前为止,尚未发表的大型多中心随机试验采用MINS作为主要终点。然而,正在进行的大型围手术期试验将MINS纳入到主要结局中。尽管MINS包括心肌梗死,但有关心肌梗死干预措施的效果可能无法对MINS更广泛的预后产生影响。
围手术期缺血评估研究(POISE)随机纳入8351例在其接受非心脏手术前2~4h使用美托洛尔100mg或安慰剂的患者进行研究。围手术期使用β受体阻滞剂可降低30%非致命性心肌梗死的风险,但会使罹患卒中的风险的几率提高2倍且会增加所有原因导致的病死率。POISE试验的发现同研究所有相关围手术期β受体阻滞剂随机试验的系统回顾相一致。β受体阻滞剂使用不同的给药方案(例如,种类、剂量、滴定策略)来安全有效的预防心肌梗死仍是可能的,但这些假设仍推测需要更正式的试验来证明。因此,目前证据表明,不应该一开始使用β受体阻滞剂来预防围手术期心肌梗死。然而,长期服用β受体阻滞剂的患者应继续服药治疗,或待手术后血流动力学稳定后再次开始服药。仍需注意的是,可能需要调整剂量来缓解术后低血压的发生。目前尚无使用β受体阻滞剂预防MINS的随机对照试验,但相关的观察性研究的综合结果并未表明有临床获益。
POISE-2试验将10010例患者随机分配接受阿司匹林或安慰剂,同时在2×2影响因素试验中分配接受α2受体激动剂(可乐定)和安慰剂。阿司匹林和可乐定两种药物都不降低心肌梗死和死亡的发生率。然而,可乐定会引起心动过缓和低血压,阿司匹林会增加出血。POISE-2试验结果也同系统综述一致,这些综述包括所有使用α2受体激动剂和阿司匹林的相关围手术期随机试验,以及有关阿司匹林预防MINS的有限参考文献。因此,这两种药物都不应一开始使用,以减少围手术期心肌梗死的发生。先前置入冠脉支架的患者应持续使用阿司匹林。
ENIGMAⅡ(对使用笑气混合气体进行麻醉的评估)试验随机纳入了7112例患者。在几项包含术后心肌梗死以心血管为结局的试验中,笑气既无好处也无明显坏处。在预防MINS方面,几项试验也比较了静脉全身麻醉(如丙泊酚)和七氟烷吸入麻醉,未发现显著的受益证据。
在其他预防MINS的干预措施中,有关他汀类药物和血管紧张素转换酶抑制剂或血管紧张素Ⅱ受体阻滞剂的数据有限。观察性数据表明,降脂治疗可能会降低围手术期心血管风险。在一项VISION研究的倾向性匹配的亚分析中,术前使用他汀类药物同MINS发生风险降低有关。然而,在使用阿托伐他汀降低手术并发症风险的试验中,随机纳入648例一直使用他汀药物的患者,这些患者有心血管疾病或有风险因素,他们在接受非心脏手术前18h被随机分配接受高剂量阿托伐他汀或安慰剂,试验表明他汀药物治疗并未降低MINS发生率。因此,尚不清楚使用他汀类药物预防MINS的好处。术前暂时停用肾素-血管紧张素系统抑制剂也可能会降低MINS的发生,但因数据仅来自于观察性研究,现有证据的说服力有限。
术前远程缺血预处理,即在下肢或前臂使用血压袖带充气膨胀超过收缩压的情况下进行短暂的循环缺血,已被探索作为降低MINS发生率的潜在策略。在一项随机纳入82例接受血管手术患者,比较患者使用远程缺血预处理和常规处理的研究中,可观察到使用远程缺血预处理可降低MINS发生率。相反,在更大的假手术对照CRIPES(在择期血管手术之前进行心脏远程缺血预处理)研究中,缺血预处理并未降低MINS发生率。因此,当前证据未能支持缺血预处理具有预防MINS的益处。
2、由手术导致的低血压
考虑到血流动力学控制是麻醉管理的关键,但术中恰当的血流动力学目标以及损伤阈值的了解知之甚少。评估由手术导致低血压的有力试验仍很少。近期大型电子数据集的分析表明,即使是短暂的术中低血压(其阈值直到最近才被普遍认可),同心肌损伤、急性肾功能损伤和病死率有关。
在一项研究中,当绝对平均动脉压≤65mmHg以及相对于基线降低30%与心肌损伤有关。对急性肾损伤,其阈值也类似。低血压的严重程度和持续时间是决定心肌损伤和病死率的关键因素。例如,一旦平均动脉压降低至55mmHg,仅仅几分钟的低血压持续时间就与病死率升高有关。收缩压、舒张压和平均动脉压对MINS有类似的预测作用。
围手术期心肌损伤并非随机发生,主要仅发生于原先存在心血管风险的患者。因此,相较于由手术导致的低血压,基线风险因素能更好的预测心血管结局。然而,低血压和MINS之间的关联是重要的。不同于患者的基线特征,血压在很大程度上是可控的。例如,大约1/3的低血压是由在麻醉诱导和麻醉结束之间的麻醉药物造成的。术中连续监测(包括动脉穿刺监测血压)可降低低血压的发生频率和严重程度。在两项随机试验中,持续血压监测检测到了更多的低血压,这能使临床医师较早进行干预,从而降低低血压和总低血压暴露的发生次数。各种无创监测系统都能可靠的连续估计血压,因此可以被认为是有创动脉血压监测的有价值的替代方法。
尽管术中低血压和MINS有很强的关联性,但为证实低血压和不良预后之间的因果关系,对降低低血压的干预措施进行随机试验是有必要的。例如,一些通常会导致低血压的围手术期干预措施(如硬膜外麻醉)并未显示会增加围手术期心脏风险。此外,由手术导致的低血压治疗并不总是简单明了。在临床实践中,缓解低血压的最佳方法仍存在不确定性,包括静脉输液的液体选择或数量、升压药的使用或选择,以及麻醉深度的管理。
目前尚未有关于血压管理策略对心肌损伤或梗死影响的随机试验数据。一项纳入298例高危手术患者比较严格控制和最低控制术中低血压的随机试验,在随机分配的实施严格血压控制组中,试验的主要结局(即全身炎症反应综合症或至少一个器官衰竭)发生率减少25%。这些发现通过一项纳入450例参与者参加的随机试验得到印证,该试验比较了常规临床治疗和血流动力学管理算法,血流动力学管理算法包括最低目标平均动脉压≥65mmHg和指导液体管理。血液动力学管理算法使中至重度心脏和非心脏并发症的相对风险降低48%,但该试验未报道术中血压,且仅发生了1例心肌梗死,故无法推断该算法对MINS发生率的影响。
3、由手术导致的心动过速
心动过速是指心率≥100次/分,其增加心肌氧需,限制冠状舒张期冠状动脉的灌注时间,并可能导致心肌损伤。鉴于心动过速对非手术性心肌梗死的影响,临床医师有理由认为由手术导致的心动过速对MINS的发生有影响,而MINS也被认为是心肌供需不匹配的结果。与该理论相一致的是,一些研究已报道了术前动态心动过速和术后MINS之间的关系。在VISION研究的二级分析中,心肌损伤与心动过速有关,当心率长期超过100次/分时心肌损伤最为明显。然而,在一项纳入近3000例非心脏手术患者的单独研究中,研究表明心率>90和>100次/分同心肌损伤没有关联。
七、MINS的术后监测 未接受手术且患有心肌梗死的患者通常具备符合一项关键诊断标准的缺血症状。然而,围手术期镇静或术后镇痛可能掩盖缺血的临床症状(如胸痛),其限制了内科医师术后诊断与患者预后密切相关的心肌梗死的能力。一项纳入2018例接受非心脏手术且处于心血管高风险患者的单中心前瞻性研究表明,仅6%术后表现cTn升高的患者有典型的胸痛症状,仅18%患者有缺血症状。类似的是,VISION研究中仅7%患有心肌损伤的手术患者表现出缺血症状,仅25%的手术患者有缺血性心电图表现。在患有MINS的患者中,术后T波倒置(17%)以及ST段压低(10%)是最常见的心电图表现,然而ST抬高(1.5%)和新发左束支传导阻滞(0.4%)并非常见的心电图表现。因此,当使用hsTnT分析时,仅有22%患有MINS的患者满足心肌梗死标准的普遍定义。 当使用传统的第四代(非高敏)cTn分析进行监测时,42%患MINS的患者符合心肌梗死标准的普遍定义。一项纳入1627例使用cTn评估的中或高风险且接受非心脏手术患者的CHASE(术后心脏健康)研究表明,315例患者患有MINS,但其中仅10例患者(3.2%)有典型的胸痛症状且仅30例患者(9.5%)术后心电图呈现缺血表现。在围手术期阶段患者大多无临床症状,且心电图异常表现持续时间短暂,因此对有效识别术后心肌损伤,进行cTn检测是有必要的。 接受非心脏手术后,使用cTn对MINS实施监测符合上述原则中的大部分。全球每年实施非心脏手术量超过3亿例,MINS的发生很常见,大约20%的外科患者会发生MINS,这取决于所使用的诊断标准和研究人群的特征。在大型前瞻性队列研究中,MINS与预后不良有显著关联,故MINS在医学上具有重要意义。心肌肌钙蛋白分析对心肌损伤有很好的敏感性和特异性。一些cTn分析方法已经产生了可供选择的预后评估阈值,在考虑筛查建议时有用。为预防MINS发生,目前尚不清楚何种干预措施安全有效,仅一项强有力的随机试验研究了可改善MINS预后的治疗策略。 鉴于绝大多数对预后有影响的MINS在没有cTn监测的情况下不会被发现,我们鼓励对特定的高危患者,在接受非心脏手术后住首个2d~3d内进行一系列cTn监测。对存在心血管事件高风险的患者,在术前进行cTn基线测量也是合理的。根据加拿大VISION研究的成本结果分析发现,为检测年龄≥65岁或有冠状动脉粥样硬化病史的高危患者的MINS而进行的TnT监测项目的相关成本不高。 加拿大心脏病学会2017年最新指南中,基于中等质量证据强烈建议对有高风险的患者,在接受非心脏手术后48h~72h内每日进行cTn测量。这些指南将高风险的患者定义为术前BNP值升高、修订的心脏风险指数评分≥1分、年龄≥65岁或年龄45~64岁且患有重大心血管疾病。欧洲心脏病学会2014年指南指出,对高风险患者可能应考虑重大手术后48h~72h进行cTn评估。欧洲麻醉学会最新指南建议,对高风险的患者应考虑在重大手术前和手术后48h~72h进行cTn评估。然而,2014年美国心脏协会临床实践指南推荐在有缺血性体征或症状的情况下进行cTn测量,但不推荐对未经选择的患者常规进行术后cTn监测。2014年美国心脏协会指南指出,对高风险的患者是否应进行术后cTn监测尚不确定。 八、MINS的预后如前所述,MINS与患者短期和长期预后不良密切相关。在一项纳入了1784项研究的系统回顾中,5项前瞻性研究报告了MINS与预后之间的关系。每项研究都表明,MINS与短期、中期和长期预后不良有关。其中几项研究还表明围手术期心肌梗死的预后相关性。例如,VISION研究中术后hsTnT浓度峰值与术后30d病死率相关。值得注意的是,在考虑术前和手术协变量后,不符合心肌梗死普遍定义的MINS和围手术期心肌梗死,与术后30d病死率独立相关。hsTnT、预估的肾小球滤过率和术后30d病死率之间无相互作用。
一项纳入2018例连续接受非心脏手术且年龄≥65岁或≥45岁有血管疾病(CAD、外周动脉疾病或既往脑卒中)患者的瑞士研究中,在术前和术后使用系统的hsTnT测量,发现有397例患者发生MINS。其中,86%被判定为与MINS一致的缺血性病因。患有MINS的患者中,术后30d的病死率为6.1%(无心肌损伤的患者病死率为1.6%),60%的死亡原因被判定为心脏方面的原因。在调整年龄、非择期手术、改良心脏风险指数评分以及住院期间的脓毒症、脑卒中或肺炎后,MINS与术后30d和1年的病死率风险增加有关。 人们普遍认为,原先曾患非手术原因导致心肌梗死的患者在出院后需密切随访。患MINS的患者在术后1至2年内也处于复发重大心血管事件和病死率的高风险中。事实上,在COMPASS试验(使用抗凝策略患者的心血管预后研究)中,参加大型随机试验患有MINS的患者比患有CAD、外周动脉疾病或两者疾病共存的稳定型的非手术患者的预后更差(91%患有CAD,63%原先有心肌梗死)。这种比较强调了出院后对MINS患者进行密切随访的重要性,以确保最佳风险分层和二级预防措施的优化。 九、MINS的术后治疗策略 MINS的术后管理仍是一个需积极进行研究的领域。虽然已确定MINS的短期和长期风险,但几乎没有对这一类高风险患者进行治疗策略评估的前瞻性研究。因此,有关MINS患者的最佳治疗策略有很大的不确定性。 MINS患者的治疗策略应根据心肌损伤的可疑原因而定。尽管大多数情况下,心肌损伤同动脉粥样硬化性心血管疾病有关,但必须考虑导致心肌损伤的其他原因。与肺栓塞、瓣膜性心脏病和急性失代偿性心力衰竭有关的心肌损伤,不应作为MINS进行处理,因为这些诊断会大大改变治疗策略。生命体征、心血管体格检查是否有杂音、颈静脉扩张和下肢水肿必须与临床风险因素相结合,以确定MINS的非缺血性原因的可能性。当对机制有疑问时,可能需要进行额外的心血管测试以进行进一步评估。例如,当怀疑深静脉血栓或肺栓塞诊断时,可考虑用经胸超声心动图检查右心室功能障碍、下肢静脉双光子超声、胸部CT静脉造影或核医学通气灌注扫描来证实诊断。 患有MINS后进行何种药物治疗方案仍不确定,但抗血栓治疗似乎是有益的。在一项纳入了415例参加POISE试验且病情进展为围手术期心肌梗死患者的事后分析中发现,出院时服用阿司匹林与术后30d病死率风险降低独立相关。这些数据与众所周知的阿司匹林作为自发性心肌梗死二级预防中的益处是一致的。 已对患有MINS的患者采取术后口服抗凝药物治疗进行分析。在MANAGE试验(接受非心脏手术后发生心肌损伤的患者服用达比加群酯)中,1754例年龄≥45岁因原先存在的缺血病因而患有MINS的患者,在事件发生后35d内被随机分配接受一日两次给予达比加群酯110mg口服,并与给予安慰剂进行比较。所有受试者术后cTn升高,并符合心肌梗死的普遍定义,或仅表现为cTn升高而无其他解释,如脓毒症、快速型房颤、肺栓塞或cTn慢性升高。阿司匹林和其他抗血小板药物由临床医师决定是否继续使用;在这两组患者中,约有2/3患者除服用研究药物外还服用阿司匹林。 在平均16个月的随访中,与安慰剂组患者相比,在主要结局(即主要血管事件综合征,包括死亡、心肌梗死、缺血性脑卒中、外周动脉栓塞、截肢和症状性静脉血栓栓塞症)方面,接受达比加群酯治疗的患者发生主要血管事件综合征的几率低。虽然威胁生命的、重大的和重要器官出血的综合情况在各组之间无显著差异,但达比加群酯增加了轻微出血和下消化道出血风险。MANAGE试验的证据表明,MINS后加强抗血栓治疗可降低长期不良心血管事件的发生率,而不会显著增加大出血的发生。尽管MANAGE的数据令人高兴,但该试验仍存在重大局限,包括患者治疗中止率高。最后,美国食品和药物管理局批准使用每天两次达比加群酯110mg的剂量,仅用于预防髋关节置换术后的深静脉血栓和肺栓塞。 目前尚无关于在MINS中运用他汀类药物的随机试验。因此,关于他汀类药物的使用建议是基于观察性数据和专家共识。在对来自POISE的围手术期心肌梗死患者的事后分析中,出院时使用他汀类药物与术后30d病死率降低有关。另外,已证明他汀类药物对非手术且已确诊患有心血管疾病包括自发性心肌梗死患者的二级预防有益处。鉴于动脉粥样硬化性血管疾病在患有MINS和围手术期心肌梗死的患者中很常见,且已知他汀类药物对患有血管疾病且处于高风险的患者有益,但不能确定益处大小。 不幸的是,动脉粥样硬化性心血管病的药物治疗似乎在MINS患者中未得到充分使用。在一项单中心回顾性观察研究中,236例患有MINS的患者中仅48%接受了阿司匹林和他汀类药物的联合治疗。在一项前瞻性单中心研究中,仅一半MINS患者接受了心脏病学顾问的治疗,几乎没有患者进行额外的心脏检查,只有29%的患者加强了指南推荐的心血管疾病的药物治疗。有必要努力提高临床医师对心血管疾病一级和二级预防的治疗指南教育以及与MINS有关的长期风险认识。在缺乏有关MINS最佳药物治疗策略的额外前瞻性数据的情况下,应强烈考虑启动或加强对假定的动脉粥样硬化性疾病的心血管风险预防治疗。在一项纳入66例患有MINS患者的回顾性观察性研究中,43例接受了心血管药物强化治疗,定义为出院时开始使用或增加抗血小板、他汀类药物、β受体阻滞剂或血管紧张素转化酶抑制剂的剂量。接受强化药物治疗的MINS患者1年内无重大心血管事件的存活率与未患有MINS的匹配手术患者的存活率相似。相反,相较于未患有MINS的手术患者,23例未接受心血管药物强化治疗的MINS患者,其死亡或心血管事件风险增加。 在符合心肌梗死普遍定义标准的MINS患者中,应根据当前临床实践指南对自发性心肌梗死患者进行指南指导的药物治疗。此外,对患有MINS和围手术期心肌梗死的患者,在其可耐受的情况下,应考虑使用β受体阻滞剂和血管紧张素转化酶抑制剂。 对患由MINS和CAD的患者进行心血管检查的作用仍不确定。MINS患者应咨询心血管病专家,是否进行心血管检测应个体化。应考虑用超声心动图评估心脏结构和功能,测量左心室射血分数,识别区域室壁运动异常,并排除存在重大瓣膜性心脏病。若对术后cTn升高缺乏其他解释,MINS患者可能需要进一步行有创或无创缺血评估,以进行心血管风险分层,并确定可能受益于冠状动脉血运重建的患者。无创性心脏成像方式包括运动或药物负荷超声心动图的功能测试,单光子发射CT或正电子发射断层扫描的核图像,或负荷磁共振成像。也可以考虑用冠状动脉CT血管造影进行非侵入性测试,以确定MINS患者CAD范围和严重程度。 对具有高风险特征的MINS患者,包括cTn水平明显升高,或符合心肌梗死通用定义的缺血症状、持续的心电图变化或新的室壁运动异常的患者,可以考虑术后进行侵入性冠状动脉造影,因此类患者的病死率和因心血管疾病再入院的风险很高。在一项纳入1093例接受非心脏手术后因围手术期心肌梗死而进行有创冠状动脉造影的患者的单中心10年回顾性观察性研究中,有589例(54%)有非限流性的狭窄,281例(26%)接受了经皮冠状动脉介入手术,73例(7%)被转为冠状动脉旁路移植手术。美国进行了一项纳入34650例围手术期心肌梗死患者的倾向性匹配队列的研究发现,相较于保守治疗,围手术期心肌梗死的侵入性治疗同住院期间较低的病死率有关,尽管在这项回顾性研究中不能排除残留的混淆因素。在患有MINS的患者中,常规进行侵入性检查不太可能有显著益处,但高危患者可能需要进行侵入性血管造影。MINS后进行冠状动脉造影的最佳时机尚不确定,可能需根据临床情况、cTn峰值升高、是否存在持续缺血以及术后侵入性血管造影的出血风险来确定。遗憾的是,针对MINS患者的心血管检测策略尚未在临床试验中得到前瞻性评估。 尽管尚无专门针对MINS患者的证据,但戒烟、提供饮食和营养咨询、鼓励减压、心脏康复和中等强度的体育活动的推荐是合理的,并优化心血管危险因素,包括高血压和糖尿病的管理。这符合目前对患有心肌梗死的非手术患者进行治疗的临床实践指南。然而,还需另外的研究来确定MINS患者二级预防的最佳方法。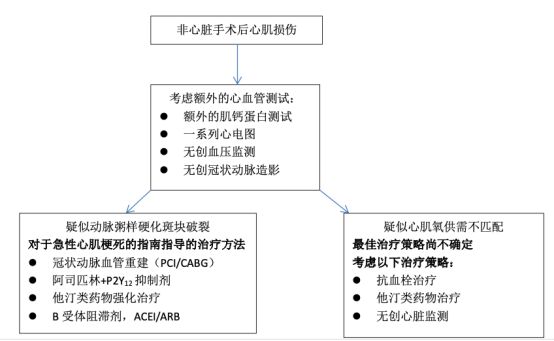
MINS于2014年首次被描述,是一个相对较新的临床诊断。有关MINS病理生理学、术前风险分层和术后管理的许多临床相关问题,尚待解决。进行可确定MINS机制的转化研究是有必要的。同MINS相关的转录组学数据可能提供机制通路等方面的的洞察,使用与MINS相关的新型生物标志物可能被用于识别处于术后缺血事件风险的患者。血小板激活、高凝状态、内皮功能紊乱和MINS病情发展之间的关系,也需更进一步的研究。因此,跨学科合作的强有力的转化工作对促进我们对MINS病理生理学的理解是非常重要的。
计划或当前正在进行的随机对照试验为预防MINS提供了新见解。例如,POISE-3是一项2×2因子随机对照试验,旨在探讨围手术期避免低血压与高血压的血压管理策略以及氨甲环酸与安慰剂对心血管事件(包括MINS)和出血的影响。POISE-3计划招募10000例≥45岁且患有心血管疾病或危险因素的成年患者,接受需要隔夜住院的重大非心脏手术。COP-AF(使用秋水仙素预防胸外科患者围手术期心房颤动)和COPMAN(使用秋水仙素预防非心脏手术后心肌损伤试验研究)正研究秋水仙素对非心脏手术患者在抗炎治疗中的潜在益处。COP-AF的主要结局是房颤,MINS是预先指定的次要结局。COPMAN是一项试点试验,主要结局是招募的可行性,次要结局是MINS。PROTECT试验(围手术期低体温和非心脏手术后心肌损伤)正在评估围手术期温度管理对随机分配到轻度低温(核心温度>35.5℃)或积极加温(37~37.5℃)的5052例成人发生MINS几率所产生的影响, 确定MINS机制的前瞻性观察性研究也正在进行。正在进行的研究将对MINS患者进行系统的冠状动脉CT血管造影,以确定显著的冠状动脉狭窄(>50%)发生率和其他发现,如隐匿性肺栓塞。尽管如此,为建立有效和安全的预防和治疗策略仍需进行其他临床试验。需行进一步的研究来确定非心脏手术后肌钙蛋白升高,是否是潜在冠状动脉疾病和供需不匹配或血栓形成的结果,并使用肌钙蛋白升高建立MINS的诊断。 十一、结论 MINS是一重要临床诊断,是通过患者接受非心脏手术后cTn值升高排除其他引起cTn值升高的非缺血性原因后,伴或不伴缺血症状或心电图异常来进行定义的。应使用本科学声明提出的MINS定义来规范临床实践和未来临床试验中对缺血事件的评估和报告。另外进行的有关确定MINS特定机制的研究对研发靶向治疗是有必要的。接受非心脏手术的高危患者应在住院期间术后48h~72h内实施一系列cTn测量。实施肌钙蛋白监测可避免MINS漏诊,且为启动二级预防措施和指导恰当的随访提供了机会。目前,在确诊为MINS的患者,尤其是原先已患有心血管疾病或那些符合现有临床实践指南治疗建议的患者中,实施加强心血管疾病二级预防的治疗措施是合理的。努力提高有关MINS的认识和理解,最终将有助于改善非心脏手术患者的术后结局。 编译 王汇贤 校订 薄禄龙 原始文献: Ruetzler K, Smilowitz NR, Berger JS, et al. Diagnosis and Management of Patients With Myocardial Injury After Noncardiac Surgery: A Scientific Statement From the American Heart Association. Circulation. 2021;144(19):e287-e305. doi:10.1161/CIR.0000000000001024 声明:古麻今醉公众号为舒医汇旗下,古麻今醉公众号所发表内容之知识产权为舒医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
减肥降压两不误,AHA科学声明教你如何双管齐下!
AHA科学声明:降低血压血脂,运动是首选、关键“治疗”!
2020 AHA科学声明:青年心肺适能—健康的重要标准
2021 AHA科学声明:改善心血管健康的饮食指导
AHA科学声明:肥胖对心血管有多重危害,腰粗也要重视!怎么减最有用?
最新 2024 版颅内静脉窦血栓形成诊断与管理:科学声明
【特色技术】超声科:肩关节疾病治疗的新思路
中医骨伤科学诊断.ppt
TAVR术后患者心脏康复研究进展
预防跑步损伤策略与建议.pptx
网址: AHA科学声明:非心脏手术后心肌损伤患者的诊断和治疗策略 https://m.trfsz.com/newsview493886.html