超说明书用药管理制度(2024)附:流程图/申报表/备案表/同意书
超说明书用药管理制度(范本)
「三级医院评审迎检必备」

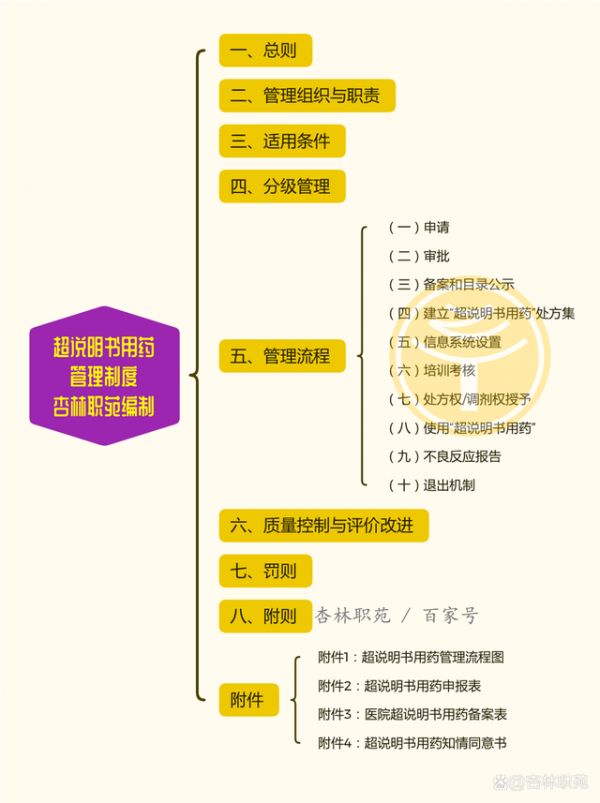
导语:为加强医院药事质量管理和药物临床应用管理,规范超说明书用药审批程序和临床应用,保障患者用药安全,降低医疗风险,杏林职苑根据《医师法》《药品管理法》《处方管理办法》《医疗机构药事管理规定》等法律法规相关规定,编制的《超说明书用药管理制度》(2024),包括总则、管理组织与职责、适用条件、分级管理、管理流程、质量控制与评价改进、罚则、总则等内容,并附流程图/申报表/备案表/知情同意书,可供医疗机构超说明书用药管理参考。
目录
一、总则
1.目的
为加强医院药事质量管理和药物临床应用管理,规范超说明书用药审批程序和临床应用,保障患者用药安全,降低医疗风险,根据《民法典》《医师法》《药品管理法》《医疗机构管理条例》《处方管理办法》《医疗机构药事管理规定》等法律法规相关规定,结合医院实际,制定本制度。
2.定义
超说明书用药,指药品使用的适应证、剂量、疗程、途径或人群等未在国家药品监督管理部门批准的说明书记载范围内。超说明书用药又称“药品拓展性临床应用”“超药品说明书用药”“药品未注册用法”“药品说明书之外用法”。
超说明书用药管理制度,指医院在遵循《医师法》《药品管理法》《医疗机构管理条例》《处方管理办法》《医疗机构药事管理规定》等法律法规和行业规范的前提下,制定适合本医院的超说明书用药管理制度,制度内容应包括管理组织、职责、适用条件、循证管理、申请、审批、管理方案、知情同意、使用情况评价及风险防控、退出机制、目录更新等。
3.适用范围
适用于医院超说明书用药管理。

二、管理组织与职责
1.药事管理与药物治疗学委员会
审批医院超说明书用药管理制度;审批临床科室提交的超说明书用药及退出申请;制定医院内超说明书用药目录;定期开展超说明书用药质控和评价工作。
2.伦理审查委员会
对临床科室提交的超说明书用药申请进行伦理审查。
3.医务部
制订、修订医院超说明书用药管理制度;临床科室上报“超说明书用药”申请材料的形式审核;汇总临床科室上报“超说明书用药”申请材料定期提交评审会审核;定期对本机构医务人员及药师进行超说明书用药培训;负责“超说明书用药”处方权和调剂权的授予与公示;组织“超说明书用药”临床用药情况的质控、评价和临床反馈。
4.药学部
参与起草医院超说明书用药管理制度;临床科室上报“超说明书用药”申请材料的收集、初审和整理;负责“超说明书用药”备案;建立“超说明书用药”处方集;整理公示通过的“超说明书用药”目录;牵头“超说明书用药”处方点评工作。
5.信息科
负责“超说明书用药”提示系统的开发和技术运维。
6.申报和使用科室医疗质量管理工作小组(以下简称科室质量小组)
对本科室范围内的超说明书用药进行全面的收集整理,及时发起超说明书用药及退出申请;对本科室超说明书用药使用情况进行监管;保护患者知情同意权并尊重患者自主决定权;用药过程中监测评估患者状况,及时上报超说明书用药相关不良反应。

三、适用条件
使用超说明书用药需要同时具备下列条件:
1.因患者治疗需要,在影响患者生活质量或危及生命的情况下,无合理的可替代药品;
2.用药目的不是试验研究,权衡利弊保障患者利益最大化;
3.有合理的医学实践证据;如有充分的文献报道、循证医学研究结果、多年临床实践证明及申请扩大药品适应证、调整剂量或途径、扩大使用人群等的研究结果等;
4.经药事管理与药物治疗学委员会和伦理委员会联合审批,紧急情况下经临床科室负责人审批,医务部、药学部备案;
本专栏《药事管理与临床药学服务质量保障与持续改进工作指引》包括药事管理与药物治疗学委员会章程(范本)和药事管理与临床药学服务核心制度等方面内容。欢迎将本专栏加入书架收藏。

相关知识
2024年健康管理师资格证报名入口官网出炉,报名流程图
深度分析:2024年各省市健康管理师考试报名流程图
疼痛科准入申报和规范化管理制度
健康管理师三级证书申报条件新变化(附学习和考试安排)
心理咨询师必备心理咨询中心常用表格、制度、方案、协议 (65份)
保健食品技术要求和说明书有哪些注意事项?保健食品常见问题与解答——注册篇(4):技术要求和说明书
健康安全环境管理体系认证证书概述与申办流程
健康安全环境管理体系认证证书 HSE申办流程及资料准备
健康管理师证书报考官网附2024最新网址(从报名到拿证全流程)
国家食品药品监督管理总局令(第22号) 保健食品注册与备案管理办法
网址: 超说明书用药管理制度(2024)附:流程图/申报表/备案表/同意书 https://m.trfsz.com/newsview505577.html