欧盟全新重磅官宣:MDR/IVDR过渡期确切时间表
欧洲时间7月17日,欧盟发布《关于非欧盟/欧洲经济区国家当局医疗器械和体外诊断医疗器械的情况说明》《Factsheet for authorities in non-EU/EEA states on medical devices and in vitro diagnostic medical devices》,具体说明MDR/IVDR过渡期修改的相关事宜,适用于非欧盟、非欧洲经济区主管当局、海关、经销商等参考和查阅。
该情况说明指出:计划向欧盟市场投放医疗器械的第三国制造商,应熟悉欧盟法规关于过渡期的规则、时间表和义务。
该情况说明书进一步解释了确切的过渡期时间表↓
MDR过渡期时间表
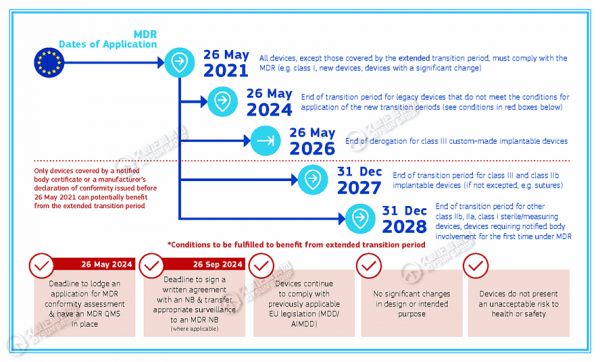
·2021年5月26日:所有器械,除过渡期延长所覆盖的器械以外,必须符合MDR(例如:I类、新器械、有重大变化的器械);
·2024年5月26日:不满足新过渡期应用条件的遗留器械的过渡期结束;
·2026年5月26日:III类定制植入器械的过渡期终止;
·2027年12月31日:III类、IIb类可植入式器械的过渡期结束(如缝合线);
·2028年12月31日:其他类IIb、IIa、I类无菌/测量器械、MDR下首次需要公告机构参与的器械的过渡期结束。
注意:仅限于2021年5月26日之前发布的公告机构证书或制造商的合格声明所涵盖的器械,才能从过渡期延长中受益。
*从过渡期延长中受益,所需满足的条件:
-2024年9月26日:提交MDR合格评定申请并已建立MDR质量管理体系的最后期限;
-2024年9月26日:与NB签署书面协议并将适当的监督转移至MDR公告机构(如适用)的最后期限;
-器械继续遵守先前适用的欧盟法规(MDD/ AIMDD);
-设计或预期目的无重大变化;
-器械不会对健康或安全构成不可接受的风险。
IVDR过渡期时间表
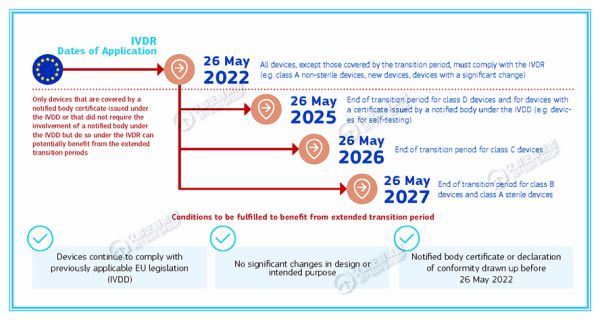
·2022年5月26日:除过渡期间所涵盖的器械外,所有器械都必须符合IVDR标准(例如:A类非无菌器械、新器械、有重大变化的器械);
·2025年5月26日:D类器械、具有IVDD下公告机构颁发的证书的器械(例如:用于自我测试的器械)的过渡期结束;
·2026年5月26日:C类器械的过渡期结束;
·2027年5月26日:B类器械和A类无菌装置过渡期结束。
注意:仅限于IVDD下颁发的公告机构证书所覆盖器械,或无需IVDD下公告机构参与但需要IVDR下公告机构参与的器械,才能从过渡期延长中受益。
*从过渡期延长中受益,所需满足的条件:
-器械继续遵守先前适用的欧盟法规(IVDD);
-设计或预期目的无重大变化;
-2022年5月26日前起草的公告机构证书或符合性声明。
→ 欢迎点击上方粉我~关注【久顺医械技术服务】医械知识不迷路!
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
《欧盟注册那些事》第六集:MDR认证路径选择技巧
超声波治疗仪的频率和功率如何影响治疗效果?
欧盟有机认证简介
欧盟有机认证(Euro
反弹!疫情下欧盟各国防控措施又有新变化!近期出口欧洲风险分析
健身教主帕梅拉官宣欧扎克:推出“新一代格兰诺拉”
拟延期6个月,完整版安评设置过渡期
重磅官宣!
马斯克的“减肥药”或有致癌风险,面临欧盟安全性审查
揭秘:欧派橱柜“Health+抗菌板”重磅发布,抗菌技术首度运用家居领域打造健康厨房
网址: 欧盟全新重磅官宣:MDR/IVDR过渡期确切时间表 https://m.trfsz.com/newsview790866.html