药品注册实现按时审评审批,新药加速上市
沪上导读:
中国药品审批时间长,向来饱受诟病!而如今当我们看到食药监总局终于“痛定思痛",在严控质量的同时,最大程度提高药品审批速度,的确是一个捷讯,但也是“几家欢喜几家忧”!因为这意味着,创新能力强的药企可凭借自身优势,抢占市场先机,而劣质药企则很可能在大浪淘沙下更快“出局”!
5月2日,国家市场监管总局发布《2018年一季度市场环境形势分析》,就一季度药品检查、打击犯罪,以及互联网+食品药品工作情况进行介绍,其中特别就行业内外关注的药品审评审批工作进行了总结。
《形势分析》介绍:2018年一季度,共审议批准66个药品品种上市,核发国产药品批准文号96个,进口药品注册证48个,港澳台医药产品注册证8个,进口药品分包装批准文号17个;完成医疗器械产品审批448项。
药品审评中心发布信息,这些获批上市的新药包括石药集团的注射用紫杉醇(白蛋白结合型)、日本大冢制药的德拉马尼片等中外知名产品。(翻至文末,看2018年第一季度药品审评中心批准上市的部分药品详情)
加快临床急需药品审评审批及上市速度,是药改的重要内容。节日期间,九价HPV疫苗(人乳头状瘤病毒疫苗)从公示拟纳入优先审评审批通道,到有条件获批上市历时6天,刷新了最快纪录。
已经让业界真切感受到了我国药品审评审批的速度。新药申报上市平均耗时8年的历史已被改变。
而根据3月22日,原国家食药监管总局发布的《2017年度药品审评报告》:2017年,我国批准上市药品394个(以药品批准文号计),其中化学药品369个,中药民族药(以下简称中药)2个,生物制品23个;国产药品278个,进口药品116个;纳入优先审评审批品种53个,占13.5%。
机构改革之初,业界曾担心药品审评审批工作会受到影响。但,从结果来看,此项工作并未受到干扰。从数据对比中可以看到,一季度药品审评中心核发批准文号169个,较之去年,有增无减。
此外,药品审评审批工作还取得了以下成绩:
药品注册申请积压已由高峰时的2.2万件降至4000件以内,各类药品注册申请基本实现按时限审评审批。
研究起草《药品上市许可持有人管理办法(试行)》,为全面推行相关制度做好准备。
深入推进仿制药质量和疗效一致性评价工作,截至2018年第一季度,已有17个品种22个品规通过一致性评价并对外公布。
积极推进药品注射剂再评价、药品品种档案建立等工作。
我国提议的“医疗器械临床评价”项目在国际医疗器械监管论坛(IMDRF)第13次管理委员会会议立项,原食品药品监管总局发布公告明确我国适用部分国际人用药品注册技术协调会(ICH)二级指导原则的相关事项,药品医疗器械监管与国际接轨的步伐进一步加快。
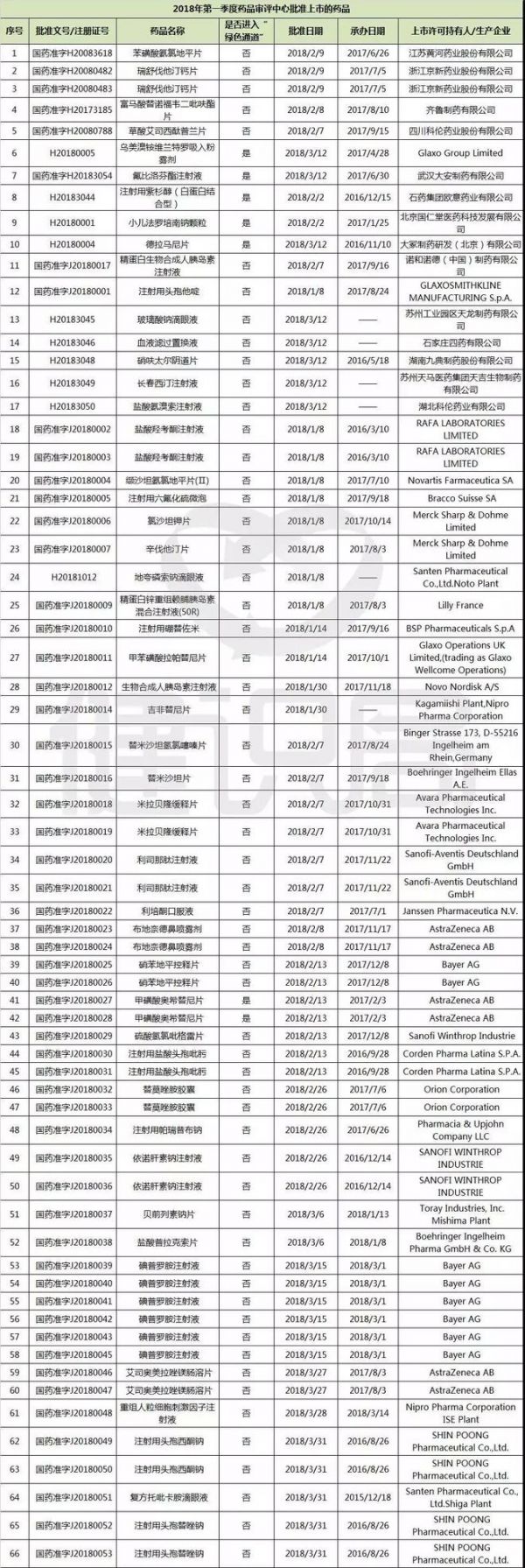
2018年第一季度药品审评中心批准上市的部分药品
特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
Notice: The content above (including the pictures and videos if any) is uploaded and posted by a user of NetEase Hao, which is a social media platform and only provides information storage services.
相关知识
药品审评审批加倍提速 新药好药上市有望加快
北京:加速创新药械审评审批
在海外,药品如何审评审批
2021年6月药品注册审评审批报告
国家药监局:深化审评审批制度改革 加快临床急需新药等上市速度
药品审批有望提速 三类药品将会被优先审批
我国药品审评审批制度改革再提速
国家食品药品监督管理总局发布《关于药品注册审评审批若干政策的公告》
国产药品如何进行注册审批
药品审批流程+受理号含义+评审时间.doc
网址: 药品注册实现按时审评审批,新药加速上市 https://m.trfsz.com/newsview1289517.html