Foxp3介导的代谢重编程增强CAR
Foxp3是调节性T细胞(Tregs)的关键转录因子,不仅在维持Tregs的免疫抑制功能中发挥核心作用,还参与调节T细胞的代谢过程。近年来的研究表明,Foxp3在调节T细胞代谢重编程方面具有重要作用,尤其是在低氧和营养缺乏的条件下,Foxp3能够赋予Tregs代谢优势,使其在免疫抑制的肿瘤微环境中保持功能。然而,Foxp3在CAR-T细胞中的作用及其对CAR-T细胞代谢和抗肿瘤效力的影响尚不清楚。
研究方法与实验设计
CAR-TFoxp3细胞的构建
复旦大学骆菲菲课题组通过将Foxp3基因与第三代CAR构建体共表达,成功生成了CAR-TFoxp3细胞。这种设计旨在通过Foxp3的表达,对CAR-T细胞进行代谢重编程,以增强其在肿瘤微环境中的适应性和抗肿瘤效力。
代谢分析
研究人员对CAR-TFoxp3细胞进行了全面的代谢分析,包括有氧糖酵解、氧化磷酸化和脂质代谢的检测。通过比较CAR-TFoxp3细胞与传统CAR-T细胞的代谢特征,揭示了Foxp3介导的代谢重编程的具体机制。
功能验证
为了验证CAR-TFoxp3细胞的抗肿瘤效力,研究人员在多种体外和体内模型中进行了实验。包括共培养实验、人源化免疫系统模型以及肿瘤小鼠模型等,以评估CAR-TFoxp3细胞的抗肿瘤效果和免疫抑制特性。
研究结果
Foxp3介导的代谢重编程
实验结果显示,CAR-TFoxp3细胞表现出显著的代谢重编程特征。具体表现为有氧糖酵解和氧化磷酸化水平的下调,以及脂质代谢的上调。这种代谢转变是由Foxp3与动力蛋白相关蛋白1(Drp1)的相互作用驱动的。Foxp3通过与Drp1结合,调节线粒体分裂,从而优化细胞的能量代谢。
CAR-TFoxp3细胞的抗肿瘤效力
在体外共培养实验中,CAR-TFoxp3细胞显示出更强的肿瘤细胞杀伤能力,与传统CAR-T细胞相比,其抗肿瘤效力显著增强。在人源化免疫系统模型中,CAR-TFoxp3细胞能够有效地抑制肿瘤生长,且未表现出免疫抑制功能。此外,CAR-TFoxp3细胞在肿瘤微环境中的适应性显著提高,其在低氧和营养缺乏条件下的存活率和功能维持能力优于传统CAR-T细胞。
免疫抑制特性的缺失
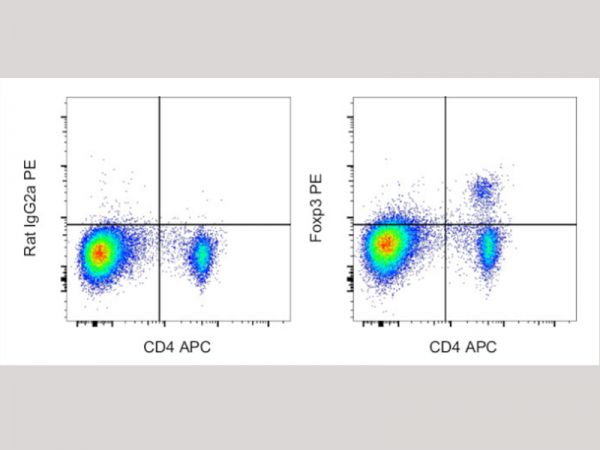
尽管Foxp3是Tregs的关键转录因子,但CAR-TFoxp3细胞并未获得Tregs的免疫抑制功能。研究人员通过多种免疫学检测方法证实,CAR-TFoxp3细胞保持了CAR-T细胞的细胞毒性功能,同时减少了免疫抑制标志物的表达。
讨论
Foxp3在CAR-T细胞中的双重作用
本研究揭示了Foxp3在CAR-T细胞中的双重作用:一方面,Foxp3通过代谢重编程增强了CAR-T细胞的抗肿瘤效力;另一方面,Foxp3并未赋予CAR-T细胞免疫抑制功能。这一发现打破了传统观念中Foxp3仅与免疫抑制相关的认知,为CAR-T细胞疗法的设计提供了新的思路。
代谢重编程对抗肿瘤效力的影响
Foxp3介导的代谢重编程通过优化CAR-T细胞的能量代谢,使其在低氧和营养缺乏的肿瘤微环境中保持高效的功能。这种代谢优化不仅增强了CAR-T细胞的抗肿瘤效力,还减少了细胞在肿瘤微环境中的耗竭和功能障碍。
临床应用前景
本研究为CAR-T细胞疗法的优化提供了重要的理论依据。通过引入Foxp3介导的代谢重编程,可以显著提高CAR-T细胞在实体瘤治疗中的疗效。未来的研究将进一步探索这种策略在不同类型肿瘤中的应用潜力,并评估其在临床治疗中的安全性和有效性。
结论
复旦大学骆菲菲课题组的研究成果揭示了Foxp3通过代谢重编程增强CAR-T细胞抗肿瘤效力的新机制。通过构建CAR-TFoxp3细胞,研究人员成功实现了CAR-T细胞的代谢优化,显著提高了其在肿瘤微环境中的适应性和抗肿瘤效力。这一发现不仅为CAR-T细胞疗法的优化提供了新的策略,也为未来癌症免疫治疗的研究开辟了新的方向。
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
莱芒生物代谢增强型CAR
莱芒生物:代谢增强型CD19 CAR
AACR速报:莱芒生物代谢增强型CAR
莱芒生物超亿元A轮融资成功,加速代谢增强型CAR
CAR不止于肿瘤治疗,CAR在感染性疾病和自身免疫疾病的新发展
疫苗增强CAR-T细胞疗法,或根除某些实体瘤
靶向CAR
【论肿道麻】Sirtuins: T细胞代谢和功能的重要调节因子
获超亿元融资,100% CR,莱芒生物代谢增强型肿瘤免疫疗法强在哪里
Nature:脂质信号转导增强了肿瘤Treg细胞的功能专一性
网址: Foxp3介导的代谢重编程增强CAR https://m.trfsz.com/newsview1696102.html

