生酮饮食(ketogenic diets,KDs)是一种超低碳,高脂肪饮食方式,备受喜爱健身及减肥人群青睐。除了能减肥健身维持体型外,研究发现生酮饮食对很多代谢疾病如糖尿病、肥胖、肿瘤等都有不错的治疗效果。但关于生酮饮食如何影响机体的代谢过程和免疫应答,发挥治疗疾病的功能目前还不清楚。多项研究指出KD可以改变宿主肠道菌群的组成和功能,但KD如何改变肠道菌群,以及肠道菌群的改变对宿主的代谢与免疫会产生怎样的影响仍待研究揭示。 2020年5月20日,来自加州大学旧金山分校微生物和免疫学系的Peter J. Turnbaugh教授的研究团队在《Cell》 上发表了题为Ketogenic Diets Alter the Gut Microbiome Resulting in Decreased Intestinal Th17 Cells的研究,报道了生酮饮食产生的βHB(β-羟丁酸)可以直接抑制肠道内的双歧杆菌(Bifidobacterial)的生长,进而降低肠道内Th17细胞的比例,调控宿主的免疫反应。

首先,作者在17位肥胖但非糖尿病患者中开展了交叉实验(crossover study)。所有受试者先进行四周基础饮食(baseline diet, BD),随后切换为四周生酮饮食(KD),在两种饮食的最后一周收集受试者粪便样品,利用16-seq分析肠道菌群组成。结果显示,KD会大幅升高受试者血清中酮体(AcAc和βHB,即乙酰乙酸和β-羟丁酸)的水平。同时,受试者肠道菌群组成有非常明显的变化,共有19个种属的肠道菌在两种饮食条件下存在显著差异,其中双歧杆菌属在KD条件下降低最为明显。
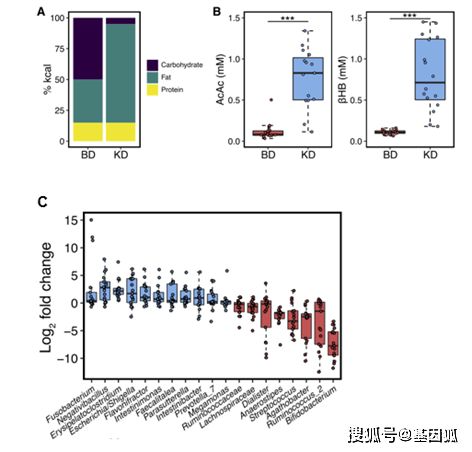 (图3.1 生酮饮食相比基础饮食使肠道菌群的结构发生改变)
(图3.1 生酮饮食相比基础饮食使肠道菌群的结构发生改变)
为了找出两种饮食方式引起肠道菌群改变的原因,作者在3个不同组小鼠中分别匹配低脂饮食LFD(78/12/10 CHO/fat/protein),高脂饮食HFD(15/75/10)和KD(0/90/10)饲喂3周,然后检测它们肠道菌群的组成。结果显示,只有KD组小鼠βHB水平是升高的,而Bifidobacterium仍然是KD组中比例下降最显著的种属。
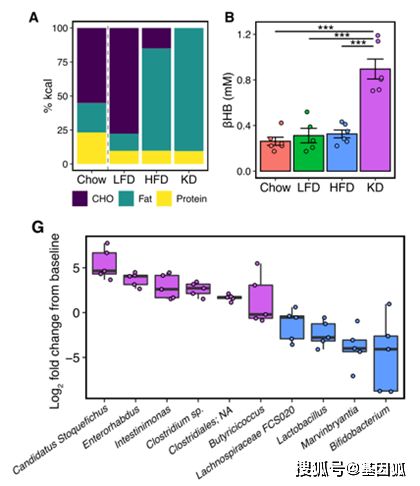 (图3.2 生酮饮食与高脂饮食对肠道菌群的不同影响)
(图3.2 生酮饮食与高脂饮食对肠道菌群的不同影响)
那么,KD是如何使肠道中Bifidobacterium比例下降的呢?根据之前的研究结果,黏液层的改变及胆汁酸的影响等诸多因素可能引起菌群组成的改变,然而作者一一排除了这些可能性,最后将关注点放在了酮体上。尽管肝脏是酮体生成的主要器官,但是小肠内皮细胞也可以产生酮体。并且,在KD中能够观察到βHB水平明显升高。体外实验结果显示,βHB可以特异性抑制Bifidobacterium adolescentis(strain BD1)菌株的生长,并且是通过改变培养基pH实现的。作者检测到小肠组织内βHB水平比肠腔内高出几个数量级,意味着在KD条件下,定植于肠道上皮细胞的Bifidobacterium可能暴露在局部高浓度βHB环境中,使其生长受到抑制。
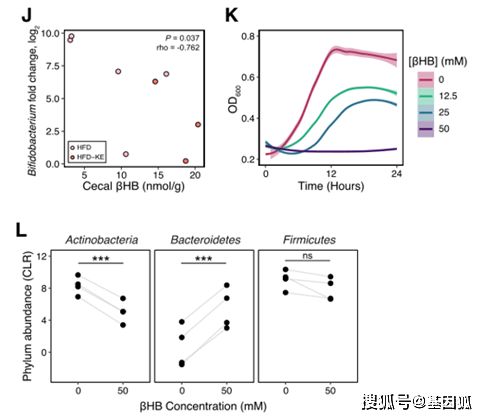 (图3.3 酮体代谢物能够直接抑制肠道菌群的生长)
(图3.3 酮体代谢物能够直接抑制肠道菌群的生长)
最后,KD引起的肠道菌群的改变对宿主来说有什么样的病理意义呢?已有研究表明,Bifidobacterium会诱导促炎的Th17细胞的表达。作者发现,在HFD饲喂组,给没有肠道微生物寄生(germ-free)的小鼠移植B.adolescentis会增加小肠内Th17细胞的比例,而在KD饲喂组进行同样的操作,并不会显著增加小肠内Th17细胞的比例。此外,分别将患者BD与KD时期来源肠道菌群移植到germ-free小鼠中,发现移植KD组肠道菌群的小鼠,其肠道Th17比率明显低于移植BD组肠道菌群的小鼠。这些数据说明,KD能够影响肠道菌群,进而影响宿主免疫。
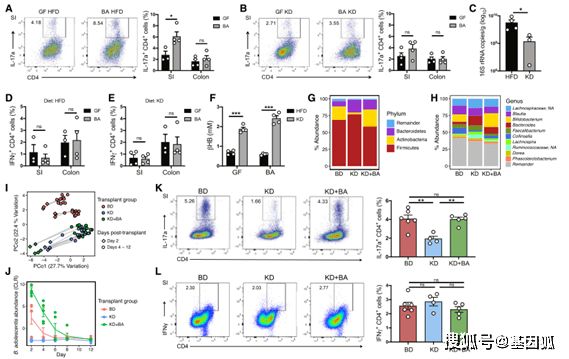 (图3.4 KD相关的肠道菌群减少germ-free小鼠体内Th17细胞的累积)
(图3.4 KD相关的肠道菌群减少germ-free小鼠体内Th17细胞的累积)
总结起来,Peter J. Turnbaugh教授团队的工作揭示了生酮饮食如何影响机体免疫,指出了肠道菌群在其中的桥梁作用,为我们提供了代谢-肠道菌群-免疫之间交流的新思路。
来源广东医科大学精准医学科学中心
返回搜狐,查看更多
责任编辑: