自 20 世纪 80 年代初以来,由聚二氧环己酮(一种合成的可生物降解聚合物)制成的医疗器械就已上市。然而,尚未发表有关其性能和安全性的评论。
本文旨在审查和评估市售聚二氧环己酮植入物及其在患者中的安全性和性能。
富临塑胶供应可吸收/不可吸收材料:
可吸收聚合物、单体、单丝、3D打印单丝、复丝、无纺布、管不可吸收单丝、复丝一、简介
医疗器械可用于诊断、治疗、治愈或预防人类和动物的疾病。考虑到医疗器械的医疗应用和材料特性,例如强度、稳定性和降解特性,可以使用多种材料来制造医疗器械。理想的医疗植入物价格实惠且易于获得,但还应提供良好的生物相容性,避免任何异物反应 (FBR)。医疗器械植入物可采用可降解材料和不可降解材料两种形式,前者在达到其功能后应降解为无毒产品。与不可降解器械相比,可生物降解器械的一个关键优势在于,它不需要进行第二次植入物移除手术,从而减少了患者就诊的次数、愈合时间和医院费用,同时还避免了潜在的长期并发症免疫反应。
通常,可降解医疗器械由聚合物制成,聚合物是重复单体的链,可以是天然的或合成的。这些类型的材料对医疗应用很有吸引力,因为它们能够定制机械性能和降解曲线,并且可以为不同的医疗目的设计官能团。与天然聚合物(如蚕丝、纤维素和壳聚糖)相比,批次之间的微小差异以及通常减少的慢性 FBR 也是合成聚合物的一个优势。不同的聚合物已经用于不同的临床应用,包括血管支架、骨水泥和伤口敷料。
聚酯是一类聚合物,其降解是由酯键的水解引起的,并且此类聚合物的降解产物通过代谢途径被再吸收。用于医疗应用的一些最常见的可生物降解合成聚酯包括聚乙醇酸、聚乳酸和聚己内酯,它们是常见缝合线和缝合锚钉的主要成分,包括 Safil® 缝合线、VICRYL® 缝合线和分别为 MONOCRYL® 缝合线。
聚二氧环己酮 (PDO) 是另一种常用于制造可生物降解医疗器械的聚酯。它也称为 PDS、聚对二氧杂环己酮、PDX 或 PDDX,是一种合成的可吸收无色聚酯,于 20 世纪 80 年代初首次生产。PDO 通常是在有机金属催化剂和热量存在下通过对二氧环己酮开环聚合来合成的(图1)。根据现有 PDO 产品提供的文献,该聚合物被认为是非抗原性和非热原性的,并且发现在植入后的吸收过程中诱导最小的组织反应。 PDO通过水解降解并在体内完全代谢。由于其相对较长的吸收持续时间(182-238 天)和合成性质,PDO 广泛用于需要持久可吸收材料的植入式染色或未染色医疗器械。PDO 是一种半结晶聚合物(约 55% 结晶),玻璃化转变温度范围为 –10℃ 至 0℃,熔融温度为 110–115℃。这些特性使得 PDO 缝合线能够在尽可能低的温度下通过挤出工艺制造,从而防止自发解聚。
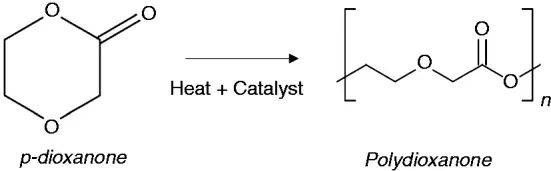
图1. 单体对二氧环己酮和聚合物聚二氧环己酮的化学结构。
在医疗领域,PDO 已被植入不同的形状和尺寸,并且多种 PDO 医疗设备已作为手术中的标准做法使用,即 PDS II 缝合线 (Ethicon) 和 OrthoSorb® 矫形针 (Johnson & Johnson International)。由于聚合物主链中存在醚氧基团,PDO 缝合线通常具有高度柔韧性。然而,尽管 PDO 装置被广泛使用,但人们仍然担心体内释放的酸性降解产物。
据作者所知,迄今为止还没有出版物概述 PDO 植入物的临床安全性和性能。为了帮助未来 PDO 医疗植入物的开发,我们审查了具有 CE 标志和/或食品和药物管理局 (FDA) 批准的 PDO 植入式医疗设备的安全性和性能结果及其在临床试验或其他医疗应用中的使用。
二、方法
01.FDA批准的PDO医疗植入物清单
我们于 2019 年 3 月使用搜索词“聚二氧环己酮”、“PDO”、“PDS”、“PDX”、“PDDX”和“poly-p-”对 FDA 510(k) 和上市前批准 (PMA) 数据库进行了搜索。 dioxanone”查找所有经批准的 PDO 植入式医疗设备。纳入标准为:由 PDO 制成的具有或不具有抗菌涂层的植入式医疗器械。排除标准为:非医疗器械、并非由 PDO 制成的器械、非完全由 PDO 制成的器械(不包括抗菌涂层)、不可植入人体的器械以及由未指定材料制成的器械。应该指出的是,正如“已上市医疗植入物及其分类”部分中所讨论的,临床数据对于提交上市前通知 510(k) 不是强制性的。 FDA 批准使用此流程的医疗器械上市是通过证实与其他已上市的谓词器械的等效性;因此,FDA 510(k) 数据库可能包含尚未商业化或临床使用的医疗器械。
对获得的结果进行分析和选择后,根据每个 510(k) 提交(如果有)中提供的实质等效关系设计了谓词树。
02.制造商和用户设施设备体验不良事件报告
从 2008 年到 2018 年,按年份对 FDA 的制造商和用户设施设备体验 (MAUDE) 不良事件报告数据库中的“FDA 批准的 PDO 医疗植入物列表”部分中列出的搜索词进行了搜索。同样的纳入和排除标准适用。如果结果既不是不良事件报告也不是产品问题报告,则也被排除。该数据库于2018年5月检索,结果数量按事件类型和年份统计。
03.医疗器械召回
FDA 医疗器械召回数据库于 2018 年 5 月使用“FDA 批准的 PDO 医疗植入物列表”部分中列出的相同搜索词进行了搜索,并分析了每份 510(k) 提交文件提供的信息。适用相同的纳入和排除标准。
04.临床研究检索策略和标准
系统地分析了 PDO 医用植入物的临床安全性。我们使用“FDA 批准的 PDO 医疗植入物列表”部分中列出的搜索词并添加 FDA 中找到的 PDO 设备的品牌名称,对 Clinical Trials.gov 和国际临床试验平台 (ICTRP) 网站进行了搜索作为额外搜索词进行搜索。还使用了四个研究数据库(MEDLINE、Embase、Scopus 和 Web of Science)。在这些研究数据库中,“FDA 批准的 PDO 医疗植入物列表”部分中列出的搜索术语与“临床试验”、“患者”、“人类”和“临床”一起使用。此外,还审查了已确定文章的参考文献。应用的纳入标准是:在患者或病例报告中进行的临床试验或研究,其中 PDO 医疗植入物代表至少一个自变量。适用于研究的排除标准是:正在进行的没有公开结果的临床试验、非英语出版物、未对人类患者进行的研究、仅限评论和摘要的出版物。这些检索于 2019 年 3 月进行。评估和比较 PDO 装置与非 PDO 装置的相关临床试验和科学出版物根据手术结果分别进行分析和评分(在线附录 1)。创建了第二个评分系统(在线附录 2)来分析所有符合纳入/排除标准的出版物。第二个评分系统着眼于不良结果的百分比和成功植入的百分比,分别评估安全性和性能。仅当结果被明确报告并与设备相关时才进行评分。两个评分系统均分析了关于材料安全的五个主要因素:手术部位感染(SSI)率、是否存在炎症反应、是否存在异物反应、是否存在术后发热和是否存在术后疼痛。根据种植体的成功情况单独评估性能水平。
三、结果
01.经监管部门批准的 PDO 设备
510(k) 数据库报告了 81 份提交材料,其中只有 47 份可以接受且与本研究相关。其余 34 份提交材料涉及的医疗器械要么含有其他聚合物,要么未植入体内,要么提供的信息不足以满足要求。可以在在线附录 3 中找到允许的设备列表。
PMA 数据库中发现的唯一 PDO 装置是 Ethicon 的 PDS 缝合线(PMA 编号 N18331),并补充了 S001 至 S027。这些 PMA 补充基于对原始设备的更改,可以包括设备本身、其包装或标签或其制造过程的更改。该缝合线的名称从 1990 年起通过补充 S022 更改为 PDS II。
根据所描述的搜索结果,PDO 医用植入物可分为四大类:缝合线、板/网、夹子/钉书钉和螺钉/别针(在线附录 3)。根据这些数据,可以看到已批准的 PDO 医疗植入物的演变图2。随着时间的推移,批准数量的增加表明,自 1981 年首次推出 PDO 以来,人们对 PDO 植入物及其在患者中的使用的兴趣持续增加。
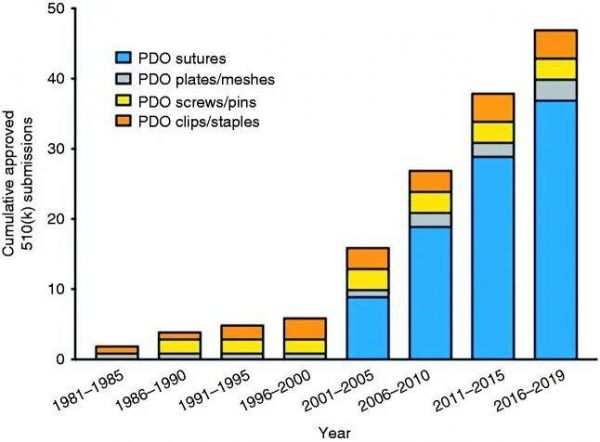
图 2. 不同类型 PDO 医疗器械的 510(k) 累计提交数量。
根据可受理的 510(k) 提交的可用信息,设计了谓词树(在线附录 4)。每个设备都基于实质等效性链接到其谓词以及它们所谓词的设备。由于 510(k) 数据库提供的信息有限,九项提交的谓词未识别。大多数 FDA 批准的 PDO 装置都是缝合线,并直接或间接连接到通过 PMA 途径批准的 PDS™ II。根据现有信息,至少有六份提交材料涉及的缝合线与其谓词的缝合线略有不同(例如,额外的缝合线尺寸)。此外,10个植入物被认为以直接方式基本上等同于非PDO设备,其中6个植入物也被认为基本上等同于其他PDO设备。
即使核心材料相同,植入物的形状、表面积和重量也会影响身体对其的反应。因此,在分析不同类型的医疗器械时应评估这些因素。在表格1,可以看出常见PDO设备在尺寸和重量上的差异。我们根据估计的 PDO 密度 1.318 g/cm³计算了每个的估计重量。应该注意的是,估计的重量是每个设备的重量,不一定对应于手术期间植入体内的 PDO 的重量,具体取决于设备的应用。
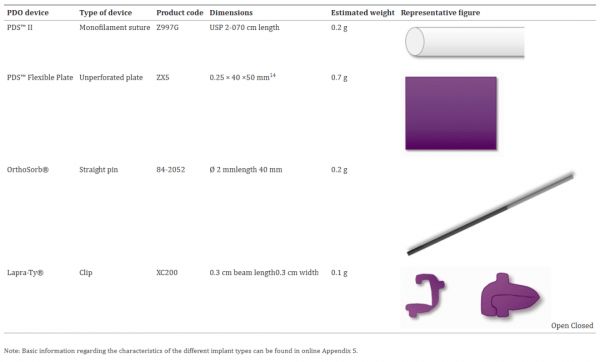
表格1. 不同类型PDO设备的尺寸、估计重量和代表图。
02.MAUDE 不良事件报告
MAUDE 数据库显示了 6859 个结果。应用纳入和排除标准后,1377 个结果被采纳。删除重复项后,搜索总计 1278 个结果,识别不良事件报告和产品问题报告。图3代表2008年1月至2018年4月(含)与PDO器械相关的不良事件报告和产品问题报告数量。可见,不良事件和产品问题的主要原因是伤害和故障。目前尚无因 PDO 植入造成死亡的报告。
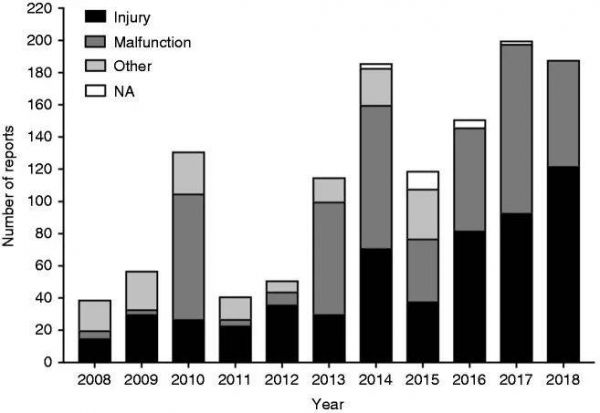
图 3. 制造商和用户设施设备体验结果按年报告涉及 PDO 植入物的不良事件和产品问题报告。不适用:不可用。
03.医疗器械召回
FDA 医疗器械召回数据库提供了 24 条结果。在应用纳入/排除标准并删除重复项后,涉及 PDO 设备的 16 起召回被视为可接受。这些内容呈现在表2。
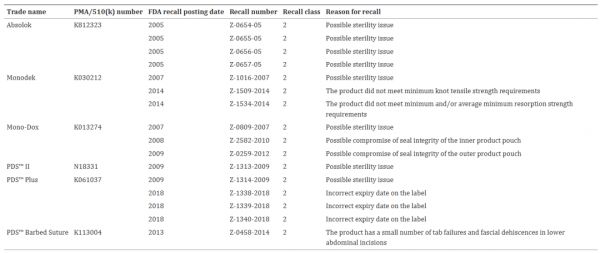
表 2. PDO 医疗器械召回。
PDS™ 倒刺缝合线 (K113004) 于 2013 年因下腹部切口中少量标签失效和筋膜裂开而被召回,而其他缝合线则因包装和无菌问题或不符合产品规格而被召回。从数据可以明显看出,这些设备均未因设备材料问题而被召回。
04.临床试验和临床研究
在删除重复项并应用纳入/排除标准后,153 篇涉及临床研究的出版物被认为是可接受的并进行了分析。在可接受的出版物中,49 篇是已发表结果的临床试验,104 篇是科学出版物。科学出版物包括回顾性研究和病例报告。出版物显示,PDO 植入物在创伤和骨科手术、耳鼻喉科和普通外科领域的报道较多。
科学出版物和临床试验根据在线附录 1 和 2 进行评分。在使用评分系统时,11 篇出版物和临床试验没有对评估的五种不利结果和表现中的任何一种发表评论,因此从分析中删除。比较不同类型的 PDO 种植体时(图4),据报告,夹子和订书钉的不良结果百分比最高,导致安全评分较低。图5表明,除 PDO 夹子和钉书钉外,PDO 设备具有超过 90% 的安全性和超过 65% 的性能功效。
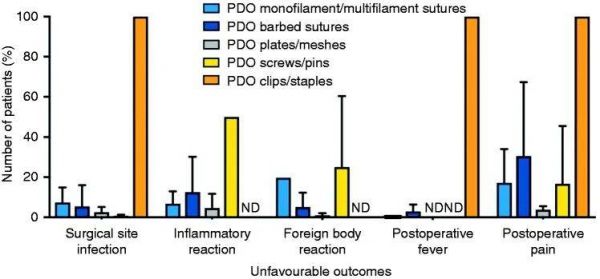
图 4. 根据种植体类型,PDO 种植体不良结果的百分比。 ND:无数据。
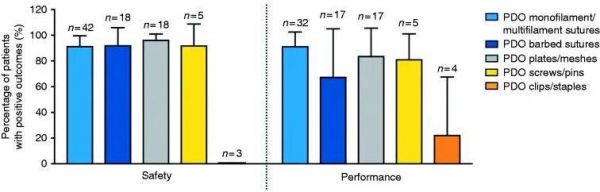
图 5. PDO 植入物的安全性和性能功效。 n:出版物数量。
图6根据在线附录1比较了PDO种植体与非PDO种植体的安全性和性能。在安全性方面,PDO种植体通常比非PDO修复具有更高的安全评分。就性能而言,总体而言,与非 PDO 设备相比,它没有差异。
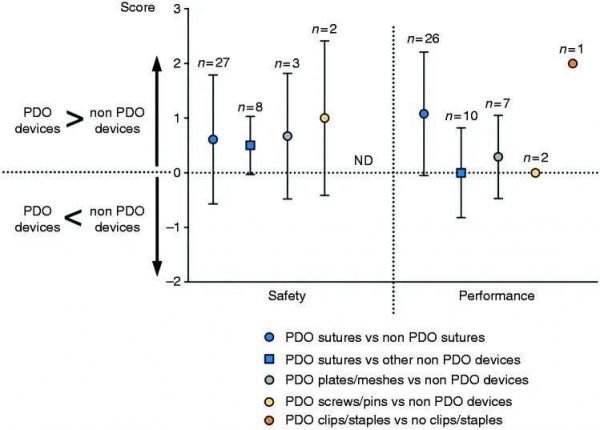
图 6. PDO 种植体与非 PDO 种植体在安全性和性能方面的比较。 n:出版物数量; ND:无数据。
富临塑胶供应可吸收/不可吸收材料:
可吸收聚合物、单体、单丝、3D打印单丝、复丝、无纺布、管不可吸收单丝、复丝四、讨论
01.市售医用植入物及其分类
自 1976 年以来,美国 FDA 监管在美国销售的所有医疗器械。FDA 流程旨在确保所有器械从开发到分销和使用的整个过程都是安全有效的。1976 年医疗器械修正案根据其风险程度将医疗器械分为监管类别:I 类、II 类和 III 类,其中后者包括最复杂和风险最高的设备。此分类过程类似于欧盟委员会在欧洲实施的分类过程(根据 2017/745 医疗器械法规定义)。大多数 II 类器械需要提交上市前通知 (510(k)),而大多数 III 类器械在上市前需要 PMA。虽然 III 类器械具有最严格的监管水平,但如果它们与 1976 年 5 月 28 日之前上市的任何其他器械基本相同,则可以通过 510(k) 途径上市,除非 FDA 要求 PMA 数据。18通过 510(k) 上市前通知途径,制造商只要能够证明其设备与已合法上市的设备基本等同,就有机会获得更快的市场批准。如果等效性声明得到证实,则该市售设备称为谓词。这种实质上的等同性基于预期用途、技术特性以及安全性和有效性。为了证明等效性,动物数据或人体临床试验结果可以作为 510(k) 提交的一部分。然而,应该指出的是,通过 510(k) 途径批准上市并不一定意味着有可用的临床数据,或者该设备之前曾在其他市场(例如欧洲)使用过。另一方面,PMA需要更详细的信息,即临床方案、不良反应和并发症、患者投诉、技术数据和非临床数据(例如毒理学、拉伸强度和保质期)。随后在 20 世纪 90 年代引入了 1976 年医疗器械修正案的补充内容,其中包括医疗器械报告,该报告使 FDA 能够接收有关重大医疗器械不良事件的信息。此外,根据 1990 年安全医疗器械法案,FDA 必须公开 FDA 510(k) 上市前审查。
如前所述,47 种 PDO 植入物通过 510(k) 途径获得批准,只有一种植入物通过 PMA 流程获得批准(在线附录 4)。这种 PMA 批准的设备(PDS™ 缝合线,于 1982 年批准商业化)被直接或间接地视为随后通过 510(k) 批准的大多数 PDO 缝合线的前提。因此,超过 97% 的 PDO 缝合线提交材料(全部在实质等效性的基础上获得批准)不一定需要详细说明产品的全面信息,例如非临床数据和/或动物/临床数据,除非 FDA 另有规定。美国食品和药物管理局。如果谓词在上市后的临床使用中引起不良反应,从而导致产品召回,这种方法可能会出现问题。然而,这并不一定意味着引用召回产品作为谓词的医疗设备也会受到调查。此外,还发现 10 个 PDO 植入物直接将非 PDO 设备作为谓词,即基于相似的功能或形状。这些植入物的供应商可能没有考虑材料和形状对这些提交材料中所需功能的综合影响,以及它们对植入后降解过程和宿主组织反应的影响。由于提交 510(k) 可能不需要动物和/或临床数据,因此在设备获得市场批准后植入患者体内之前,不会评估宿主组织反应和可能的不良反应。最后,由于九个 PDO 医疗植入物没有关于其谓词的公开数据,因此作者不可能评估谓词的适用性。
正如“PDO 降解过程”和“FBR 和炎症反应”部分所述,植入物质量会极大地影响生物相容性。表格1显示 PDS 板比对比 PDO 种植体更重,并且 Lapra-Ty® 具有最低的重量和尺寸。设备的形状、尺寸、表面特征、重量和机械完整性会影响宿主组织与不同植入物的反应,即使它们是由相同的材料制成的。因此,设计植入物时需要考虑这些参数。
已批准的 PDO 植入物对患者安全性和有效性的影响将在“安全评分系统 - 测量结果”部分中进一步讨论。
02.MAUDE 不良事件报告
MAUDE数据库仅限于过去10年内的不良事件报告。该数据库包含自 20 世纪 90 年代初以来的所有自愿报告、用户设施报告、分销商报告和制造商报告。制造商和进口商有责任在发现有合理理由表明其医疗设备之一导致死亡或严重受伤或发生故障的信息时提交报告。
检查时图3不同类型的 PDO 植入物存在大量故障和伤害报告(1278 份报告),但考虑到每年植入 PDO 装置的患者数量(相比之下,在同一时期),这一比例很小,发现了 4000 多份关于 VICRYL® 缝合线(仅由聚乳酸 910 制成)的报告)。此外,不可能说这些报告的事件是由医疗器械材料或形状引起的,而不是由所使用的外科手术或技术造成的。这是因为,在大多数情况下,无法回收医疗设备进行调查,或者 FDA 无法提供或提供更多信息。这些不良事件和产品问题报告均未声称 PDO 设备与任何患者死亡有关。
03.医疗器械召回
当设备有缺陷和/或对健康构成风险时,就会发生医疗设备召回。有时,这意味着设备只需要检查、调整或修复,并不意味着产品已停产或从市场上撤出。召回可分为三个不同的类别:I 类(产品有合理的机会导致严重的健康问题或死亡)、II 类(产品可能会导致暂时或可逆的健康问题,或者有轻微的机会导致严重的健康问题或死亡)。严重的健康问题或死亡)和 III 类(产品不太可能导致任何健康问题或伤害)。 FDA 医疗器械召回数据库包含可追溯至 2002 年 11 月的召回报告。
因为可以看出表2,这些设备均未因设备材料问题而被召回,因为设备的化学成分不会影响密封或包装完整性,也不会影响最终规格的满足,因为这是制造过程中每个产品质量控制过程的一部分。关于PDS™倒刺缝合线的召回,筋膜裂开可能是由缝合线上的倒刺沿手术切口破裂筋膜引起的。目前尚无该产品是否仍在市场上的信息,并且在线搜索中也找不到该产品。
04.PDO降解过程
在考虑 PDO 植入物的生物相容性和使用时,了解 PDO 的生物降解过程非常重要。可生物降解植入物的降解过程应与植入组织的愈合速度完美匹配,从而在需要时保持装置的机械性能。7降解过程可能发生在植入后,但也可能在制造过程中开始,此时 PDO 被熔化和/或挤压成所需的形状。这种初始降解可能导致分子量降低,因此在制造过程中应尽量减少水分和高温,以防止聚合物性能发生变化并进一步影响产品的保质期。
PDO 等吸湿性聚合物可被水解,产生降解副产物(如乙醛酸盐),这些副产物可通过尿液排出,或通过柠檬酸循环代谢形成二氧化碳和水。几位作者还报道了草酸、丙二醇、2-羟基乙酸和乙醛酸作为降解产物。由于局部 pH 值降低,乙醛酸的释放可能导致慢性炎症反应。此外,这种酸性环境可能是由于降解产物的突然快速释放或由于存在大量物质或较大表面积而引起的。4与其他聚合物(例如 PLA 和 PGA)相比,PDO 降解产物的酸性较低,因此可能引起较少的炎症反应。
生物材料的降解受到周围区域和组织的影响,即受到所涉及的机械力、疾病或健康状态以及血管化的影响。23除了可能同时发生的任何化学反应外,高应力环境产生的微观结构裂纹还可能导致暴露表面积增加和机械强度损失。19在降解的早期阶段,水渗透植入物的大部分,破坏非晶相中的化学键。6 , 7该步骤减少了长聚合物链,降低了平均分子量并增加了多分散性。此时,植入物的总体材料特性仍然保持不变,因为它们是由不受影响的结晶区域定义的。6平均分子量的降低通常发生在观察到任何材料损失之前。24在降解的最后阶段,水会水解小的水溶性碎片,导致聚合物质量、分子量和物理性能损失。6 , 25– 27然后,产生的降解产物很快从周围流体的表面去除。然而,在设备内部,降解产物无法扩散,从而形成酸性环境,从而导致酯键加速水解。这个过程解释了为什么低孔隙率植入物可能比高孔隙率植入物降解得更快,并且具有更低的功能寿命。
生物材料的降解还取决于测试对象的基础代谢率,人类的降解速度比实验动物慢。使用 PDO 缝线的体外研究表明,在缓冲溶液中放置 10 周后,缝线仍保留其 96% 以上的重量。在体外测试 PDS™ II 缝合线时,Ooi 和 Cameron 还观察到,材料在前两天会出现初始水合作用,随后是长达 20 天的休眠阶段,此时系链开始断裂。接下来是活跃阶段,持续长达 60 天,此时拉伸断裂强度和应变下降,吸水率增加。林等人。据报道,使用 PBS 缓冲液中的 PDS™ 缝线水解 14-28 天后,拉伸强度损失约 67%,42-60 天拉伸强度损失较低。7然而,就质量吸收而言,60 天时仅吸收了 1.5% 的质量,而 90% 的拉伸强度已经消失。在某些情况下,缝合线达到其目的后留下的这种材料可能会导致 FBR 和肉芽肿形成7,但一旦材料完全降解,这种结果就会消失。据报道,PDS™ 缝线在 117 至 240 天内完全吸收,在植入后 14-28 天拉伸强度损失 67%。PDO 夹子可能需要 180 多天才能完全降解。据报道, 20 个PDO 针在动物模型中植入后 3 个月和 6 个月时可见 80%,并在 24 个月时完全吸收。此外,降解产物的体外毒性可能与体内生物相容性不匹配。在一项体内研究中,93% 的 PDS™ 缝线降解产物在尿液中被去除。其他研究也表明,PDO 在兔子体内具有良好的生物相容性和积极的生物安全性。
05.安全评分系统 – 测量结果
根据设备的形状和类型,在报告 PDO 植入物使用的临床试验结果和科学论文中对 SSI、FBR、炎症反应、术后疼痛和发烧进行了分析。由于作者评估了不同的结果,因此不同论文之间没有统一的评估。因此,术后发热和疼痛被认为是与 SSI 和 FBR 不同的结果,因为作者可能没有明确将 SSI 和 FBR 定义为术后发热和疼痛的原因。基于这些结果,我们开发了两种评分系统:一种根据报告不良反应的患者百分比评估 PDO 植入物(在线附录 2),另一种评分系统比较 PDO 与非 PDO 植入物(在线附录 1)。在本节中,我们将解释植入材料如何影响上述五种结果。
手术部位感染据 Gabriel 等人称,在美国,每年约有 200 万人因住院而受到感染,每年导致 9 万人死亡。SSI 发生率可能受到不同因素的影响,包括患者的一般状况(如年龄、健康状况和合并症)、病原菌的存在、术前缺乏皮肤消毒、手术器械污染以及因长期住院而继发的院内感染留下来。
由于细菌定植和长时间连续植入,植入式医疗器械也可能导致 SSI(称为植入物相关感染)。这种细菌定植可能导致多层生物膜的形成,从而导致植入装置的故障以及随后的移除。这种生物膜还可能导致对宿主防御机制和抗生素治疗的高抵抗力。材料表面特性对于细菌粘附非常重要,即与细菌特性(细菌疏水性和细菌表面电荷)相互作用时的表面化学成分、表面粗糙度、表面构型和暴露面积。医疗器械,特别是缝合线,已经发展到通过添加抗菌涂层来尝试防止高感染率;然而,关于其效率的信息存在矛盾。医疗器械的粗糙度和构造在细菌粘附中发挥着重要作用,因为多项研究表明,表面不规则性会促进细菌粘附。这表明,与单丝缝合线相比,多丝缝合线由于其表面积更大,可能更容易引起与植入物相关的感染。然而,化学成分也会影响细菌粘附:体外和动物实验表明,与钛和钴铬植入物相比,聚甲基丙烯酸甲酯 (PMMA) 制成的植入物更容易引起感染,其可以与材料特性例如表面电荷和疏水性相关,如先前所讨论的。
图4显示 PDO 缝合线、网片/板和螺钉/销钉的 SSI 率较低(低于 10%),这可能是由于孔隙率低和暴露区域光滑所致。关于 PDO 夹子/钉书钉,两份病例报告中报告了 SSI。 Brusky 和 Tran 报告称,一名患者在使用 Lapra-Ty® 夹子锚定聚乳酸缝合线时,在顺利进行右腹腔镜经腹膜 Anderson-Hynes 肢解肾盂成形术五周后出现尿路感染。进一步研究证实 Lapra-Ty® 夹已迁移至输尿管,这可能是所述泌尿道感染的原因。芬利等人。还报告了一名患者的 Lapra-Ty® 夹子迁移,这也可能导致所报告的感染。
FBR与炎症反应炎症反应和 FBR 是生物材料植入后预期的组织反应。炎症反应被定义为血管活体组织对局部损伤的反应,即使植入材料无毒、无免疫原性且化学惰性,仍然可能引发炎症反应。炎症反应可分为两个阶段:急性炎症和慢性炎症。每个阶段都有特定的细胞类型、持续时间和总体生物学重要性。这一过程已被广泛研究和审查。急性炎症可能是由植入医疗设备时引起的组织损伤引起的,并且是正常伤口愈合过程的一部分。在此阶段,血液蛋白(如白蛋白、抗体和纤维蛋白原)被吸附到医疗器械表面。装置的化学和物理特性(例如表面化学和疏水性)将极大地影响吸附蛋白质层的组成。正是材料表面上各种血浆蛋白的呈现,为随后一系列炎症细胞的附着和激活创造了高亲和力基质,而不是材料本身。此外,物质电荷可能直接影响巨噬细胞和多形核中性粒细胞的粘附。
对于长期或永久不可降解的植入物,炎症反应通常会演变成慢性反应,从而改变植入物周围的细胞群。在此阶段,单核细胞衍生的巨噬细胞是主要细胞类型,它们会尝试分解、封装和去除植入的材料,同时重塑周围的细胞外基质。对于可生物降解的植入物,在某些情况下可能会出现慢性炎症,并且由于水解酶以及活性氧和氮的释放而加速降解,从而降低了聚合物的分子量。这样,慢性炎症可能会对永久或长期应用中植入装置的功效产生负面影响。值得注意的是,当使用可生物降解材料时,这种反应会受到时间和影响范围的限制。当植入物被吸收时,炎症和FBR会逐渐减少直至消失。已经开发了几种方法来解决炎症和医疗设备问题,包括使用生物惰性表面和生物活性策略。
医疗设备的植入还会引起非特异性免疫系统对异物的初级反应,称为 FBR。通常,FBR 是炎症和伤口愈合反应的终末期反应,但它们可以同时发生。FBR 由材料相关和材料无关的过程组成,当局部组织无法清除聚合水解碎片时,可以诱导 FBR。通常,合成材料不会引起特定的生物反应。生物材料的 FBR 涉及异物巨细胞和肉芽组织成分。植入物的表面特性、形状以及植入物表面积和体积之间的关系会影响 FBR 的成分。例如,高表面积与体积比的植入物和多孔材料(例如板和网)将在植入部位具有更多数量的巨噬细胞和异物巨细胞。另一方面,单丝缝合线等光滑表面植入物会导致植入部位出现更多纤维化组织。在炎症和伤口愈合的早期阶段,由于设备的非天然化学和物理特性,巨噬细胞在粘附到植入物表面时被激活。粘附的巨噬细胞和异物巨细胞可能导致生物材料降解并可能导致设备故障。如果存在大块材料, FBR 还会导致缝合线挤出和排斥以及缝合脓肿。这种经皮消除是通过浅层缝合线放置和增加缝合材料的质量来辅助的。FBR 可能在植入物的整个使用寿命期间持续存在于组织-装置界面处,但吸收后仅保留结缔组织。
图4结果显示,有倒刺和单丝/复丝缝合线的炎症反应和 FBR 率低于 20%,PDO 板/网片的炎症反应和 FBR 率低于 5%。尽管 PDO 板是体积最大的装置,但据报道,与其他装置相比,它们在较小比例的患者中引起 FBR,这是没有预料到的,因为多孔且体积较大的装置预计会有更多数量的相关巨噬细胞和异物巨细胞。这种差异可能与植入这些装置的宿主组织的高血管分布和低流动性有关,例如在鼻重建期间。关于 PDO 螺钉/销钉,Kalla 和 Janzen 描述了一名患者因 Orthosorb® 引起的 FBR 和炎症。这种类型的 PDO 针在单独的拇囊炎切除术中被植入双脚。第二次手术后仅在右脚观察到 FBR 和炎症。 Kalla 和 Janzen 认为观察到的 FBR 可能是由植入部位的低血管分布和温度引起的,也可能是由于第一次手术后对 Orthosorb® 的免疫过敏所致。然而,值得注意的是,这是现有出版物中唯一报道的使用 Orthosorb(R) 进行 FBR 的病例。没有论文报道植入 PDO 夹/钉书钉后炎症反应或 FBR 的发生率。还值得注意的是,在分析的 142 项临床研究中,据报道只有 0.2% 的患者患有 FBR。
术后发烧报道的术后发热发生率各不相同,但预计 13-14% 的患者会出现发热。图4结果表明,单丝/复丝和倒刺缝合线术后发热低于 4%,优于报道的比率。如前所述,PDO 夹因夹子移动而导致术后高烧。任何审查的出版物均未报道植入 PDO 板/网和螺钉/销钉后的术后发热评估。值得注意的是,在分析临床试验结果和科学出版物时,在数据分析中,手术后 48 小时内出现的发烧(通常是良性且自限性的,可能与手术相关)之间没有区别。随后出现发烧(更有可能是感染原因)。正常宿主防御机制的中断(例如医疗设备植入)是发生其他可能导致发烧的合并症的风险因素。
术后疼痛植入 PDO 板/网片的患者报告术后疼痛的比例不到 4%,这是预料之中的,因为这种类型的植入物报告的 SSI、炎症反应和 FBR 水平较低。然而,单丝/多丝缝合线 (17%)、有倒刺缝合线 (31%) 和螺钉/别针 (17%) 的疼痛程度较高。有倒刺的缝合线可能比单丝缝合线引起更多的局部疼痛,因为它们的倒刺附着在周围组织上以将缝合线保持在适当的位置。
06.临床试验和科学出版物的手术结果
在分析不利结果的百分比时(图4),临床研究显示 PDO 缝合线、板/网和螺钉/针的 SSI 和术后发热的比例较低。 PDO 螺钉/销钉的 FBR 百分比较高,其次是单丝/多丝缝合线,然后是有倒刺的缝合线。图4还显示PDO夹子/钉书钉的SSI、术后发热和术后疼痛发生率较高。这些安全性结果仅基于三份已发表的 Lapra-Ty® 缝合夹病例报告,总共三名有肾盂肾炎(肾脏炎症)病史的患者。在这三个病例报告中,观察到夹子移动,导致报告的疼痛和发烧。正如其他工作所建议的,本次综述中分析的61 份病例报告可能不能代表这些缝合夹的使用。这也意味着,并不是这些设备是由PDO制成的,导致了这种生物反应,而是设备功能的故障。然而,这需要进一步调查。仅发现一项研究报告了 Lapra-Ty® 夹子的良好性能。
总体而言,PDO 种植体在超过 90% 的情况下是安全的,并且在超过 80% 的情况下对于缝合线、板/网和螺钉/销钉的性能符合预期。 PDO 有倒刺缝合线的性能有效率较低 (67%),在分析报告使用此类 PDO 缝合线的临床研究时,两个病例报告描述了由于倒刺附着到邻近组织和手术方法以及混杂而导致的性能失败合并症,清楚地表明在这些情况下,有刺缝合线的性能不受所用材料的影响。
图6比较 PDO 植入物与非 PDO 装置的安全性和性能。结果表明,PDO 植入物显示出比非 PDO 设备安全水平更高的趋势。在某些情况下,PDO 装置与不可降解的植入物相比,可能会导致长期 FBR,从而降低其安全率。未发现任何出版物报告涉及 PDO 夹子/订书钉的安全结果。就性能而言,PDO 缝合线的性能优于非 PDO 缝合线,但与网片或手术胶水相比,其性能也同样好。值得注意的是,在评估缝合线性能的 25 篇论文中,其中 7 篇将 PDO 有刺缝合线与非 PDO 单丝缝合线进行了比较。对于有倒刺的缝合线,倒刺附着在组织上,将缝合线锁定到位并防止切口打开,与非 PDO 光滑单丝缝合线相比,这通常会提高 PDO 缝合线的性能值。与非 PDO 修复相比,PDO 板/网还显示出性能水平提高的趋势。
与非 PDO 替代品相比,PDO 螺钉/销钉具有相似的性能,但应注意,只有少数临床研究报告了这些类型设备的性能。仅发现一份出版物将 PDO 夹子/钉书钉(Lapra-Ty® 夹子)与非 PDO 修复进行比较,其性能得分为 2 分。从如此少量的出版物中,不可能推断出这些类型设备的一般性能,因为这还取决于设备的应用以及外科医生使用它的方式。
07.医疗植入物的未来
PDO 植入物传统上是通过挤压制造的,但在考虑前面提到的设计植入物的不同方面时,可以使用不同的技术。还应考虑制造过程,以尽量减少机械性能的变化(除非这些是预期用途所需的),特别是如果主要成分是水解材料。 PDO 植入物的制造应尽可能降低湿度,以免加速降解。制造过程中的过高温度也会改变 PDO 的机械性能。由于这些原因,制造商不应通过高压灭菌或干热对 PDO 医疗器械进行灭菌,但应考虑使用环氧乙烷,因为这种聚合物也对伽马辐射敏感。在制造过程中可以使用添加剂来扩大工艺规模或减少降解,但必须注意对生物安全的潜在影响。本次审查假设 PDO 植入物中不残留任何添加剂。
08.本研究的局限性
值得注意的是,FDA 声称,仅凭医疗器械报告数据不能得出与器械相关的问题的存在、严重性或频率的结论,并且如果事件周围的情况尚未发生,则在器械和不良事件之间建立关系尤其困难。已验证或设备尚未直接评估。本文分析了临床研究,以提供有关此类植入物安全性的更多信息。我们评估了所有相关出版物,但我们知道每个临床出版物中的患者人数可能无法代表植入 PDO 装置的一般人群。此外,当比较由不同材料制成的植入装置时,不同的降解率(如果适用)和植入部位可能会影响观察到的结果。
此外,尽管某种医疗器械获得了FDA的批准,但这并不意味着它目前正在市场上销售。此外,由于保密原因,无法获得医疗器械技术信息,例如降解情况、分子量、进行的动物测试。这种透明度的缺乏使得医疗器械在人体应用过程中的整体评估变得更加困难。
五、结论
PDO 医疗植入物具有不同的形状、尺寸和配置,广泛应用于许多不同的外科专业。此次审查的结果表明,没有任何产品因所使用的材料而被召回,也没有 PDO 植入物导致患者死亡。此外,患者使用 PDO 植入物产生的不良反应比例较低,这表明 PDO 缝合线、板/网和螺钉/销钉可以安全使用,并且性能符合预期。使用 PDO 夹子/订书钉时必须小心,以便正确使用,因为功能故障可能会导致 PDO 夹子移动并引起不良反应。与非 PDO 修复相比,PDO 植入物通常是安全的,并且性能至少与替代品一样好。
该综述表明,作为一种可生物降解聚合物,在考虑宿主组织的生物特性以及设备的形状和尺寸的同时,PDO 是一种安全材料,可用于开发进一步创新的可生物降解医疗植入物。
富临塑胶供应可吸收/不可吸收材料:
可吸收聚合物、单体、单丝、3D打印单丝、复丝、无纺布、管不可吸收单丝、复丝邮箱:li@fulinsujiao.com
公司地址:广东省东莞市樟木头镇塑金国际1号楼810
 返回搜狐,查看更多
返回搜狐,查看更多