全球首创:中国原研iPSC细胞疗法开启渐冻症治疗新纪元
引言:直面“绝症之王”的科学挑战
肌萎缩侧索硬化症(ALS,俗称“渐冻症”),是一种致死性的神经退行性疾病。其病理特征为大脑和脊髓中的上、下运动神经元进行性丢失,导致患者肌肉萎缩、无力,最终因呼吸衰竭死亡。目前,ALS被公认为全球最难攻克的疾病之一,患者中位生存期通常为3-5年。
在这一严峻的临床未满足需求背景下,2025年,中国生物医药企业士泽生物自主研发的异体通用型诱导多能干细胞(iPSC)衍生神经前体细胞注射液(XS228),相继获得美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)的临床试验许可(IND),并顺利完成首例患者给药。这一进展标志着中国在iPSC衍生细胞药物治疗神经系统重大疾病领域,正式进入全球第一梯队,并使该方案有望成为ALS治疗领域同类首创(First-in-Class)的突破性药物。
里程碑:中美双报双批与全球化临床启动
XS228的研发进程展现了高效的全球化开发策略,短短数年间完成了从概念验证到注册临床的关键跨越:
第一阶段:监管认可与孤儿药资格
2023年11月:XS228获得美国FDA授予的孤儿药资格认定(Orphan Drug Designation, ODD)。这是全球首个获此认定的用于治疗ALS的iPSC衍生细胞产品。该认定意味着产品在上市后享有7年市场独占权,并可享受研发税费减免及加速审评等政策支持。
第二阶段:中美双批,同步推进
2025年2月(美国):XS228正式获得FDA临床试验许可(IND),获准在美国开展注册性临床试验。2025年5月(中国):XS228获得中国NMPA临床试验许可(IND)。值得注意的是,该申请以“零发补”形式一次性获批,彰显了监管机构对其药学数据(CMC)及临床前安全性数据的高度认可。同一款中国原研细胞药物,在中美两大全球最严格的监管市场同步获得准入,验证了其技术标准与国际接轨,为未来数据的全球互认奠定了基础。
第三阶段:注册临床启动与首例给药
前期探索(IIT):士泽生物联合上海市东方医院等中心,完成了研究者发起的临床试验(IIT)。随访数据显示,XS228在ALS患者中表现出良好的安全性,并初步提示出延缓疾病进展的潜在疗效,为注册临床试验提供了关键的概念验证。
注册临床(IND):2025年9月,由北京大学第三医院牵头,樊东升教授担任主要研究者(PI)的XS228治疗ALS的多中心、随机、对照I/II期注册临床试验正式启动,并完成全球首例受试者给药。
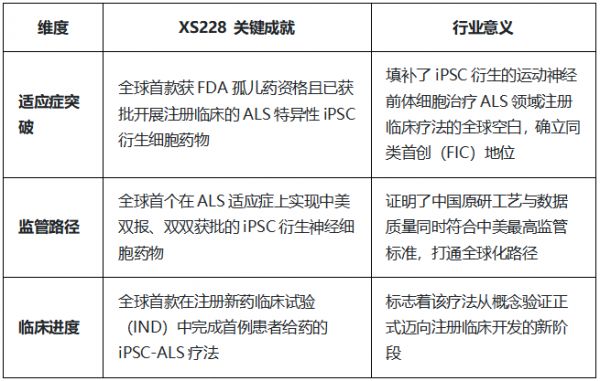
定义全球新标杆
在全球iPSC药物研发竞赛中,XS228凭借以下三项核心指标确立了其领先地位:
理性展望:挑战与未来
尽管进展令人振奋,但科学界仍需保持审慎乐观。XS228目前处于I/II期临床试验阶段,主要目标是评估安全性、耐受性及初步有效性。细胞治疗作为“活体药物”,仍面临诸多挑战:
· 长期安全性:需长期随访以排除致瘤性、异位分化等潜在风险。
· 疗效确证:需在更大样本量的随机对照试验中,验证其对ALSFRS-R评分(肌萎缩侧索硬化功能评分)及生存期的改善是否具有统计学显著性。
· 规模化生产:如何保持异体通用型细胞在不同批次间的质量均一性,仍是产业化关键。
目前,该临床试验正在招募受试者(入组标准包括:18-75岁,确诊ALS,病程≤24个月,用力肺活量FVC%≥70%等(详见士泽生物公众号,临床招募中渐冻症相关信息)。
XS228的全球化推进,不仅是中国生物医药原始创新能力的有力佐证,更展示了中国在解决全球性医学难题中的担当。从中美双批的监管突破,到顶尖临床中心(北京大学第三医院)与科学家团队的紧密协作,再到患者群体的积极参与,多方力量正共同推动这场针对“绝症之王”的攻坚战役。对于数以万计的渐冻症患者而言,每一项严谨的科学进展,都是黑暗中的一束光。XS228的旅程才刚刚开始,但它已清晰地指明了一个方向:通过再生医学的力量,让“冻结”的生命重新焕发可能。
免责声明:本文所述内容基于公开资料,细胞治疗存在个体差异及潜在风险,相关药物尚未获批上市,请在专业医生指导下参与正规临床试验。本文不构成任何医疗建议或投资推荐。
相关知识
全球首创:中国原研iPSC细胞疗法开启渐冻症治疗新纪元
全球首例!徐沪济教授团队成功应用 iPSC-CAR-NK 细胞治疗重症难治性 dcSSc
首款口服斑秃新药、「渐冻人」症创新疗法…获批上市
中国基因与细胞治疗研究突飞猛进!国内多家基因、生物技术企业展露锋芒
单次治疗脂肪厚度减少27%,酷塑中国上市开启冷冻减脂新纪元
博雅干细胞一周资讯:科学家揭示衰老抑制T细胞抗肿瘤免疫机制
干细胞技术:医疗史上第三次健康,21世纪细胞治疗时代即将来临
【技术】诱导多能干细胞(iPSC)的生产初探
颠覆传统!负熵密码糖尿病治疗仪开启血糖调理新纪元
细胞和基因治疗:创新疗法的新方向
网址: 全球首创:中国原研iPSC细胞疗法开启渐冻症治疗新纪元 https://m.trfsz.com/newsview1913173.html